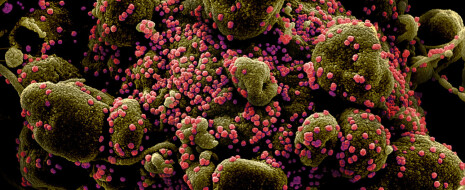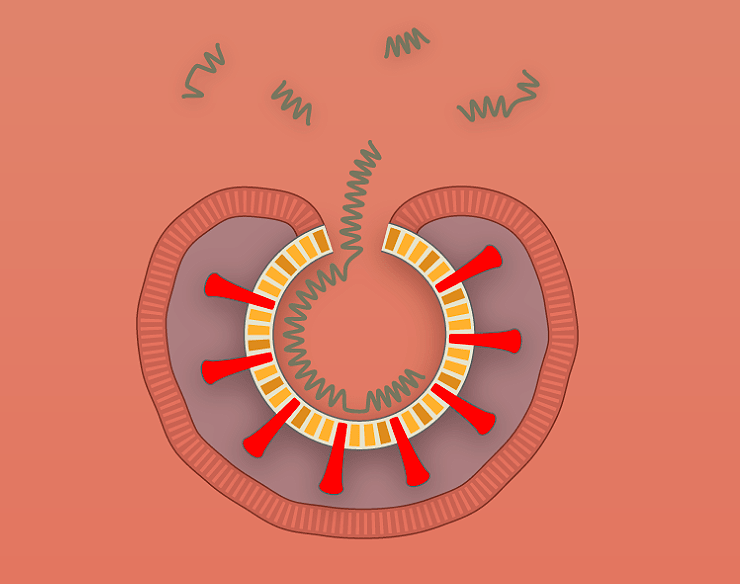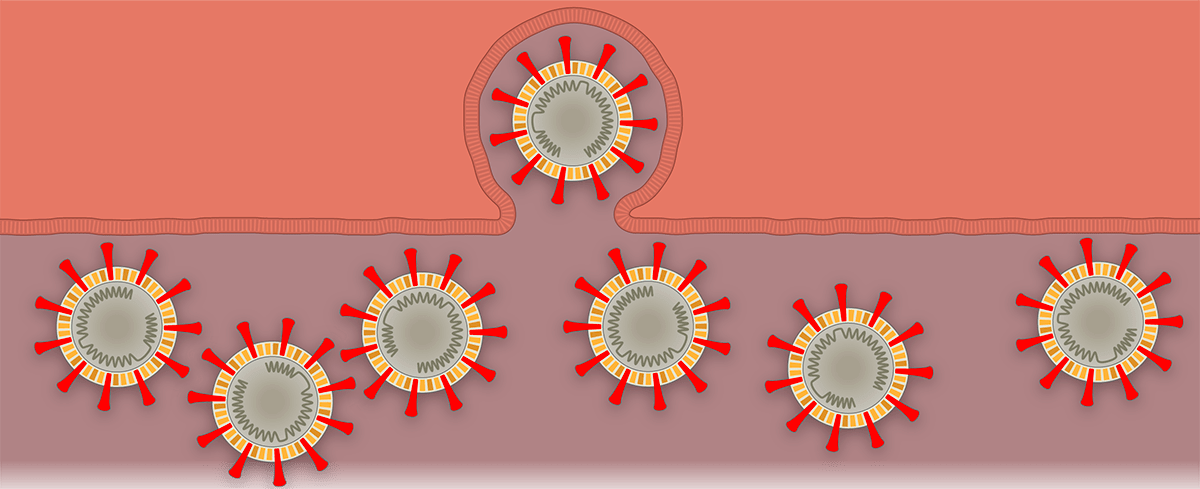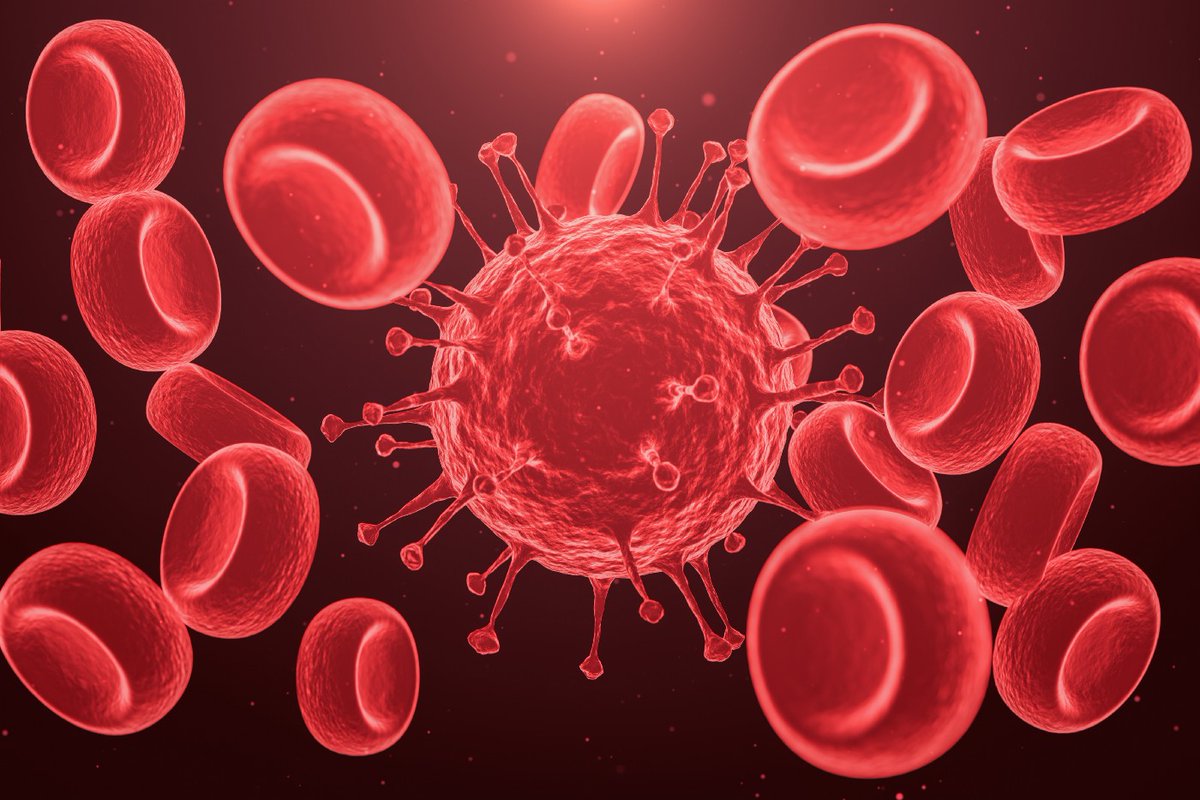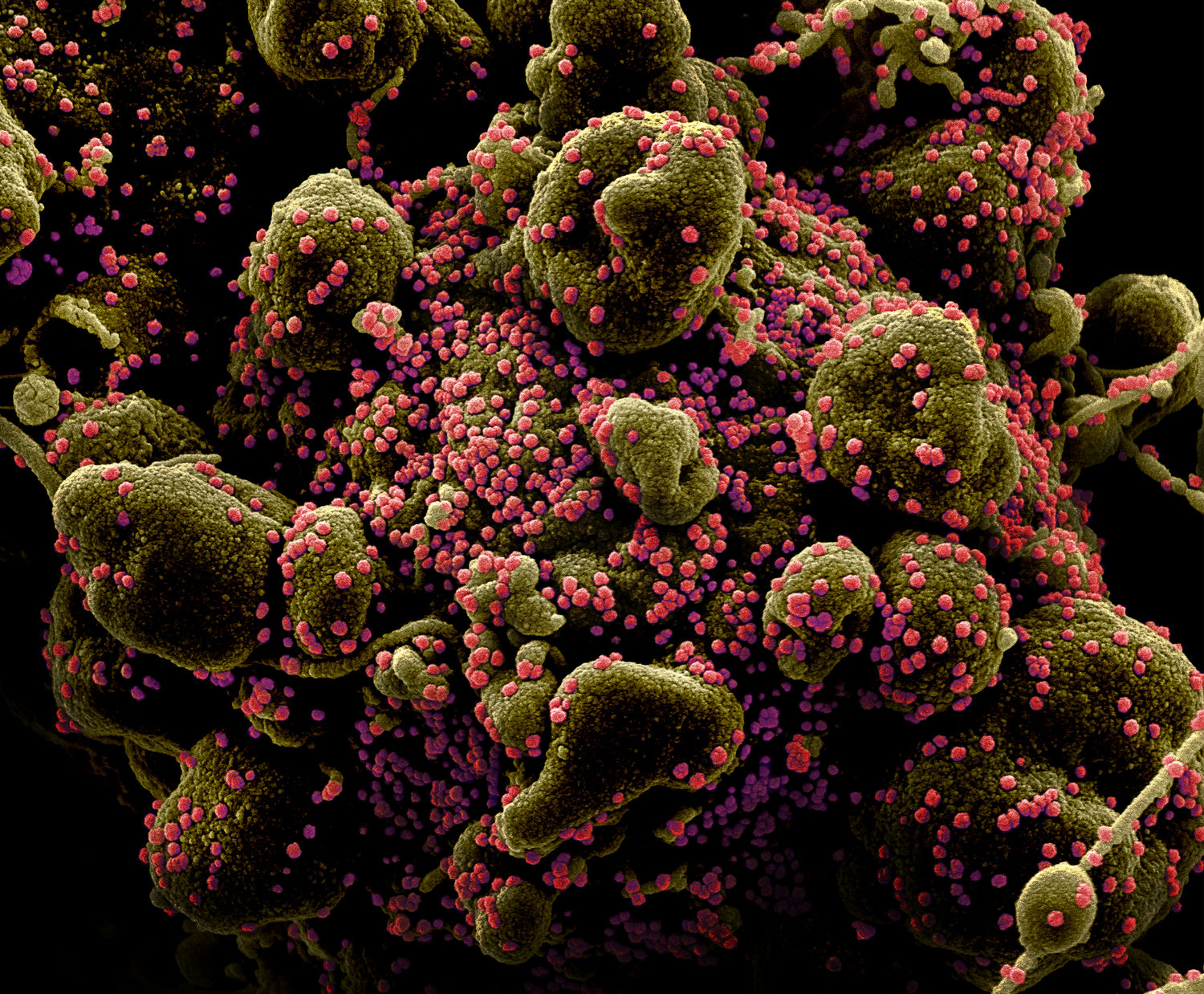
Клетка (зеленая) в окружении вирионов SARS-CoV-2 (розовые). Многочисленные выросты клетки говорят о том, что она находится на конечной стадии апоптоза — программируемой клеточной смерти — и скоро будет фрагментирована. Заражение клетки вирусом — один из поводов для апоптоза. Раскрашенная фотография, полученная с помощью сканирующего электронного микроскопа, с сайта npr.org
От публикатора: Новый коронавирус отличается резкой дихотомией течения и исхода болезни, очень лёгкое, почти бессимптомное и, наоборот, крайне тяжёлое, с плохой перспективой и разнообразными осложнениями, в т.ч. диабет, кишечные и неврологические. Приводятся материалы, какие физиологические механизмы определяют первое или второе, что, как и когда «переводит стрелку» между ними.
COVID-19: что мы знаем и чего не знаем
Содержание
- 1 COVID-19: что мы знаем и чего не знаем
- 2 1. Откуда взялся SARS-CoV-2?
- 3 2. Что особенного в этой эпидемии?
- 4 3. Сколько штаммов вируса выявлено и что это значит?
- 5 4. Что происходит с вирусом SARS-CoV-2 в организме?
- 6 5. Какие хронические заболевания повышают риск тяжелого протекания заражения?
- 7 Кто входит в группу риска?
- 8 6. Какими методами борются с вирусом сейчас?
- 9 7. Что является наиболее вероятными мишенями для будущих терапий?
- 10 8. Как обстоят дела с вакциной?
- 11 9. Какие стратегии применяют сейчас государства для защиты от эпидемии?
- 12 10. Какова ситуация в России?
- 13 Что же можно сказать о сценариях развития ситуации в России?
- 14 11. Как не допустить развития пандемий в будущем?
- 15 12. Как SARS-CoV-2 влияет на фарминдустрию?
- 16 13. Есть ли хоть что-то позитивное в эпидемии SARS-CoV-2?
- 17 P.S.: 14. А вирус точно не из лаборатории? И вообще, это точно все не мировой заговор?
- 18 Литература
- 19 Сильный иммунитет, слабый иммунитет, риски тяжёлой формы болезни COVID-19
- 19.1 Как определить риск такой реакции, и что, собственно, происходит с иммунитетом?
- 19.2 Что делать иммунитету, если не хватает подходящих Т-клеток?
- 19.3 Важны ли антитела [3], которые производят В-клетки, начиная со второй недели инфекции?
- 19.4 Как же тогда сработают терапевтические антитела к коронавирусу?
- 19.5 Есть ли у SARS-CoV-2 особенные механизмы подавления иммунитета, неправильной активации иммунитета?
- 19.6 Прививка BCG: проще ли протекает COVID-19 у вакцинированных?
- 19.7 Что почитать про упомянутые механизмы иммунитета
- 20 Возможно, иммунный ответ на коронавирусную инфекцию уникален
- 21 COVID-19 может оказаться сосудистым, а не респираторным заболеванием
«Биомолекула» продолжает отвечать на вопросы, связанные с эпидемией коронавируса SARS-CoV-2, и на этот раз рассматривает вирус с точек зрения биологии, медицины и фармацевтической индустрии. Для этого мы проконсультировались с шестью экспертами в этих областях…
Если в предыдущей статье [1] мы рассматривали бытовые вопросы, в целом направленные на превентивные меры борьбы с вирусом , то сейчас мы ищем ответы на вопросы медицинского и биологического характера, но находим их не всегда. Читайте ниже о том, что же уже известно научному сообществу, а насчет чего еще ясности пока нет.
Ситуация с коронавирусом столь актуальна в эти дни, что мы открыли на «Биомолекуле» новый раздел SARS-CoV-2, а также публикуем уже четвертый материал по этой теме. Первые три вот такие: «2019-nCoV: очередной коронованный убийца?» [2], «Хроника распространения SARS-CoV-2» [3] и «COVID-19: отвечаем на вопросы» [1]. Эта статья уже четвертая и, может статься, не последняя…
1. Откуда взялся SARS-CoV-2?
Китайское правительство сообщило о первых случаях «пневмонии неизвестной этиологии» в Ухане 31 декабря, но вирус появился в Китае на несколько недель раньше.
В январе количество случаев заражения в Китае начало быстро нарастать, в стране ввели карантин в нескольких крупных городах [4]. Параллельно вирус стал распространяться сначала по разным частям региона (китайские специальные административные регионы Гонконг и Макао, Тайвань, Япония, Корея, Сингапур), затем первые случаи обнаружили в США и Европе (во Франции). Сейчас уже несколько недель как именно Европа стала эпицентром эпидемии. Ситуация же в Китае стабилизируется, и власти заявили, что жесткий карантин в Ухане планируется снять 8 апреля. Тем не менее есть вероятность наступления второй волны заболевания, как случилось, например, в Гонконге (китайском SAR): туда возвращаются его жители, которые не могли вернуться раньше из-за карантина, и завозят вирус снова. Подробно об истоках вируса и хронике эпидемии «Биомолекула» уже писала [2], [3].
Команда исследователей показала, что геном вируса, выделенного у группы пациентов с атипичной пневмонией после посещения Уханя, на 89% совпадает с вирусом летучих мышей SARS-like-CoVZXC21 и на 82% — с человеческим вирусом SARS-CoV [5], эпидемия которого случилась в 2002–2004 годах. По этой причине вирус получил название SARS-CoV-2 [6]. Также геном вируса совпадает на 96% с геномом вируса летучих мышей RaTG13 (GenBank Sequence ID: MN996532.1)
Если у вас возникают сомнения в естественном происхождении вируса, ознакомьтесь с постскриптумом к этой статье.
2. Что особенного в этой эпидемии?
Стоит отметить, что эпидемии и даже пандемии случаются с человечеством довольно регулярно (о некоторых из них «Биомолекула» писала: «Объяснена различная вирулентность вирусов гриппа — возбудителей “испанки”» [7]), и переход вируса с животного на человека — тоже не редкость. Например, если даже вспомнить недавние случаи, вирус Зика передается через укус комара [8]; вирусы, вызывающие другие опасные заболевания SARS и MERS, попали к человеку через мясо диких животных (природные носители этих вирусов — летучие мыши); названия птичьего и свиного гриппов говорят сами за себя; заразиться вирусом Эбола можно при контакте с естественными жидкостями из организмов, например, обезьян, которые в свою очередь подхватили вирус от крылановых [9]. Но есть ли что-то необычное в эпидемии SARS-CoV-2?
«Особенность в том, что она случилось в XXI веке, — комментирует вирусолог Андрей Летаров. — Существенно изменились возможности человечества по борьбе с такими инфекциями. Изменились и этические установки: принято считать, что сейчас жизнь отдельного человека стала более важной ценностью для общества, чем, например, в XX веке. И можно предположить, что в середине XX века на такую эпидемию мало бы внимания обратили, лишь потом в семейных преданиях говорили бы, что “когда твоя бабушка была молодая, ходила какая-то страшная болезнь”.
Если сейчас не делать вообще ничего по предотвращению эпидемии, то потери, в сухом бухгалтерском подсчете, не будут очень большими, по сравнению с ежегодной смертностью от других причин. Биологически ничего экстраординарного в этой эпидемии нет.
Возможно, на мой взгляд, особенностью этого вируса является то, что для заражения нужно совсем небольшое его количество. Это рассуждение основано на том, что при таких симптомах люди продуцируют мало инфекционных аэрозолей (из чего можно было бы сделать вывод, что передаваться вирус должен не очень хорошо), но коэффициент R0 [«базовая способность к размножению», среднее количество людей, которых может заразить один носитель вируса — прим. автора] при этом больше двух. Основной способ передачи вируса, как указывает ВОЗ, — контактный или капельно-контактный, значит, “доза” вируса, необходимая для заражения, низка. И это объясняет также и проблемы с диагностикой: концентрация вируса в разных биологических жидкостях больного довольно низка, и обнаружить его может быть сложно».
Сейчас никто не знает, сколько будет продолжаться эпидемия SARS-CoV-2, но, предположительно, вспышки заболеваемости могут продолжаться в зимний сезон и после основной эпидемии [10]. Еще некоторые предположения о том, какие биологические особенности нового коронавируса «помогли» ему вызвать такую глобальную эпидемию, можно прочесть в статье Why the coronavirus has been so successful [11].
3. Сколько штаммов вируса выявлено и что это значит?
В статье в National Science Review от 3 марта 2020 года ученые при анализе 103 геномов вируса выделили два штамма: типа L и типа S, причем указали, что более агрессивный L мутировал из S [12]. Позднее они сделали апдейт: употребление термина «агрессивный» было неверным и вводящим в заблуждение (misleading). Сейчас, даже после анализа гораздо большего количества сиквенсов, все еще трудно точно сказать, насколько значимы различия штаммов коронавируса для течения и исхода COVID-19. Возможно, чтобы окончательно ответить на этот вопрос, понадобится немало времени.
«SARS-CoV-2 — это РНК-содержащий вирус, который в силу особенностей своего воспроизводства достаточно часто подвергается мутациям, — рассказывает вирусолог Андрей Летаров. — Уже сейчас наблюдается несколько десятков различных генетических линий вируса, причем их филогения (родственные отношения) хорошо коррелирует с местом выделения изолятов, то есть распространение вируса по планете происходит в масштабах времени, сопоставимых с накоплением генетических изменений в его геноме. Однако не все мутации имеют сколько-нибудь существенное значение. В определенной обстановке та или иная мутация может иметь больший репродуктивный успех, и тогда этот вариант получит большее распространение в определенной местности. И тогда мы сможем говорить о появлении нового штамма. Важно, чтобы это были не просто отличия по последовательности, но и отличия, которые сопряжены с изменением экологически важных свойств вируса, например, его контагиозности или тяжести заболевания, которое он вызывает.
Я, как и другие биологи, надеюсь, что варианты вируса, которые дают менее заметные проявления, будут приобретать большее распространение в популяции. Например, сейчас, на волне психического напряжения, связанного с эпидемией, люди стали гораздо серьезнее относиться к симптомам ОРВИ, и если раньше можно было наплевать на кашель и небольшую температуру и пойти работать, то сейчас люди всё меньше и меньше начинают так себя вести, значит, меньше заражают окружающих, и вирус медленнее распространяется. Поэтому логично предположить, что если появится вариант вируса, который дает менее выраженные клинические симптомы, которые люди не очень замечают, то это обещает вирусу больший репродуктивный успех, поскольку его “задача” — не убить как можно больше людей, а распространиться как можно более широко. Поэтому есть основания считать, что в данной ситуации по мере развития эпидемического процесса будут появляться такие формы вируса, заражение которыми будет проявляться всё меньше и меньше. Чем больше людей переболеет, включая тех, кто перенесет инфекцию бессимптомно, тем больше будет коллективный иммунитет [о нем мы поговорим ниже — прим. автора] и тем скорее это все закончится.
В целом, сейчас вообще не стоит особо обращать внимание на информацию о количестве штаммов: пока прошло мало времени с начала эпидемии, мы толком не знаем, какие свойства разных типов вируса есть и какие будут найдены».
4. Что происходит с вирусом SARS-CoV-2 в организме?
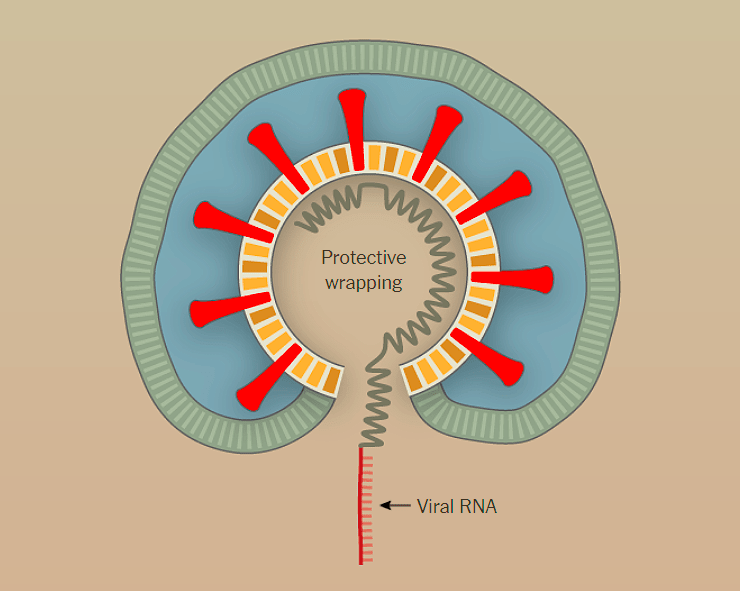
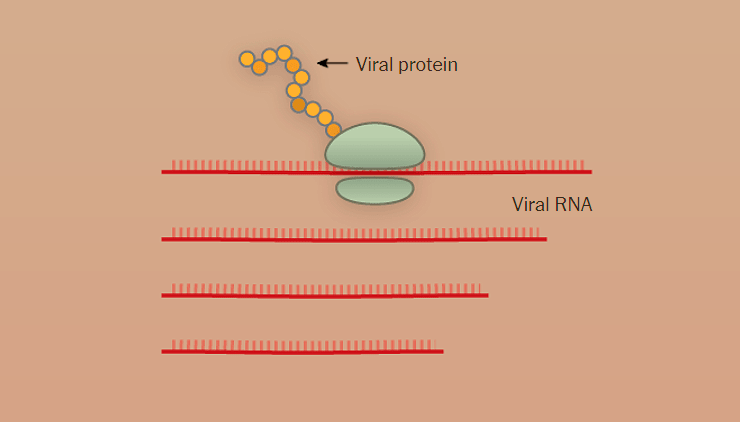
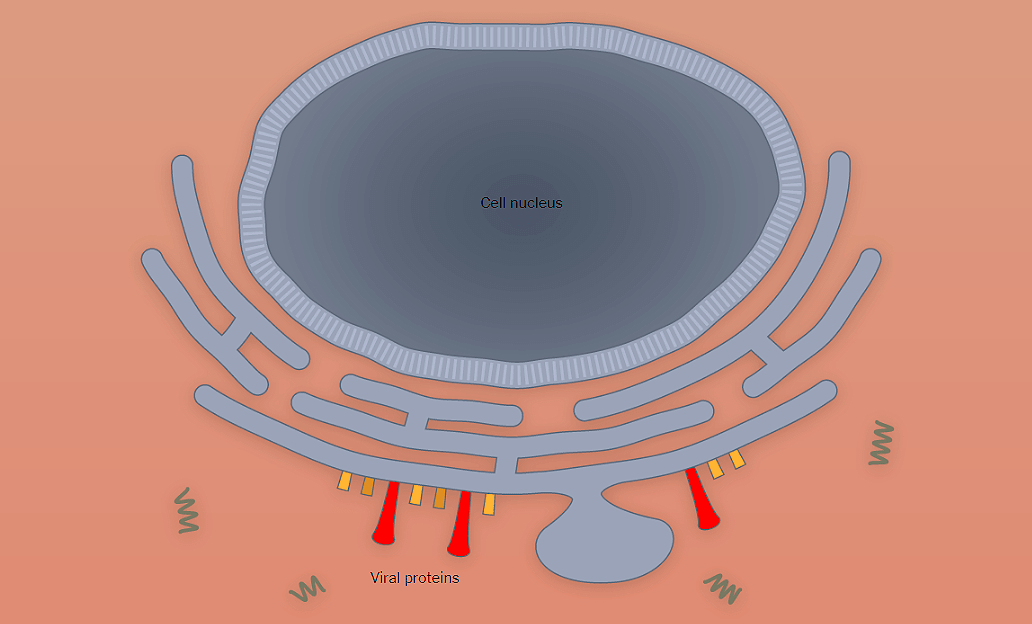
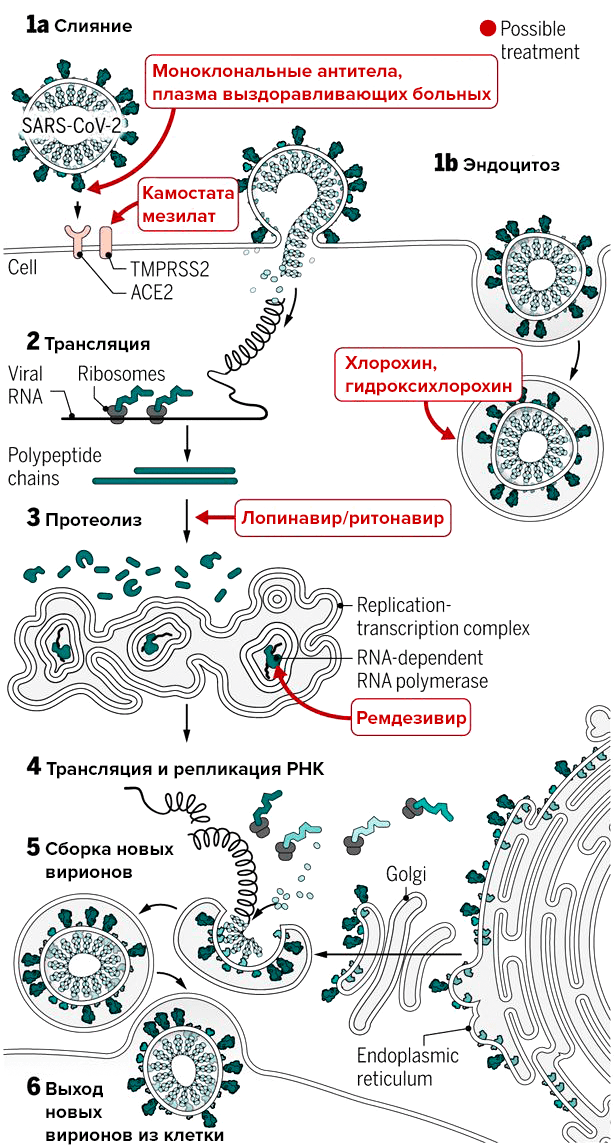
Наглядно попадание вируса в клетку, образование новых вирионов и распространение вируса по организму показано поэтапно на рисунке 1 с использованием графики The New York Times.
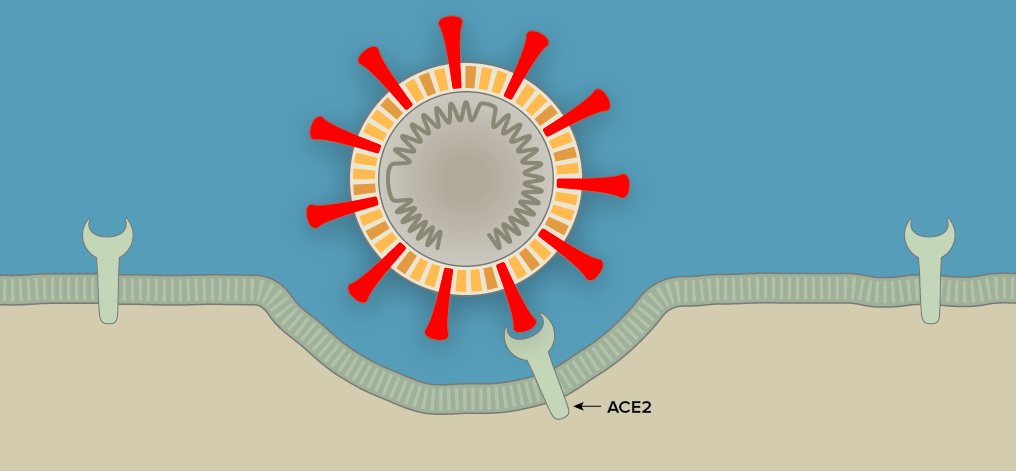
Рисунок 1а. Заражение SARS-CoV-2 клеток человека. SARS-CoV-2 проникает в организм через нос, рот или глаза, добирается до дыхательных путей и прикрепляется к альвеолярному эпителию (рецептор коронавируса — ангиотензинпревращающий фермент 2, ACE2) [13]. После того, как рецептор-узнающий белок Spike связывается с рецептором, вирусная частица попадает внутрь клетки путем эндоцитоза.
Источник Биомолекула.ру
Сильный иммунитет, слабый иммунитет, риски тяжёлой формы болезни COVID-19
Люди по всему миру болеют новой коронавирусной инфекцией. Одни переносят легко, другие тяжело, с угрозой для жизни — какие тут факторы важны и какова роль иммунитета? Есть накапливающаяся статистика: все уже запомнили, что риски тяжёлого течения COVID-19 сильно растут с возрастом пациента, значительно выше для мужчин, чем для женщин, выше для людей с астмой, заболеваниями сердца и почек, для тех, кто принимает сартаны (распространённое лекарство для лечения артериальной гипертензии) и т.д. Но эти разрозненные факты не особо помогают понять патогенез, т.е. как развивается болезнь, и выделить важные факторы выздоровления или наоборот, проявления тяжёлой формы COVID-19.
Есть основания полагать, что большинство смертей от коронавируса связаны с чрезмерной и разрушительной реакцией иммунной системы, а не с прямыми повреждениями, которые организму наносит размножающийся вирус.
Как определить риск такой реакции, и что, собственно, происходит с иммунитетом?
Иммунная реакция на вирус отличается у разных людей уже с первых часов заражения, она зависит и от наследственных факторов, факторов среды (например, загрязнённый городской воздух) и от привычек (например, курения или занятий спортом), влияющих на состояние иммунитета слизистых оболочек дыхательных путей. У кого-то быстро вырабатываются интерфероны — первые сигналы для организма о необходимости противовирусной защиты. В идеальной ситуации сигнал интерферонов I типа приводит к тому, что эпителий сам защищается от репликации вируса, и вдобавок иммунные клетки приходят и уничтожают заражённые клетки, которых на первой стадии немного. Если выработка интерферонов происходит с задержкой, вирус успевает размножиться, и для борьбы с ним требуется больше активирующих сигналов иммунитету, воспаление развивается интенсивнее/стремительнее, что приводит к — бóльшему повреждению ткани (эпителия альвеол лёгких).
Хорошо изучено, что для разных вирусных инфекций очень важен тайминг продукции интерферонов I типа. Ранняя выработка интерферона или системное введение дополнительного экзогенного интерферона (на ранних асимптоматических стадиях болезни) в моделях на животных защищает от различных вирусов (первого SARS-коронавируса, хорошо изученной модельной инфекции LCMV, вируса иммунодефицита обезьян): ткань, подвергающаяся атаке инфекции, и врождённый иммунитет справляются с первой порцией вируса сразу после заражения. А вот если продукция интерферонов I типа начинается с задержкой, вирус успевает размножиться и распространиться по площади органа и дальше по организму. В тех же моделях на животных такая динамика ассоциирована со сниженным числом Т-киллеров субпопуляции CD8+ и патологически сильным системным воспалением — организм сильнее повреждается из-за действия врождённого иммунитета, и в таком случае становится гораздо сложнее полностью избавиться от вируса.
У вируса Эболы, например, есть белок VP35, ответственный за подавление выработки интерферона, поэтому Эбола сразу переходит на второй тип динамики вирусного иммунного ответа. Из других респираторных вирусов пандемический штамм гриппа 1918 года тоже отличался нехарактерным для большинства сезонных штаммов гриппа эффективным подавлением продукции интерферонов I типа и параллельно повышал, как считается, уровень воспалительных сигналов (цитокинов) в системном кровотоке, что приводило к тяжёлому устойчивому воспалению ткани лёгких.
Параллельно и чуть позже выработки интерферонов, происходит реакция клеток врождённого иммунитета [1], в первую очередь, нейтрофилов и макрофагов. Цели этой фазы иммунного ответа (будем считать второй фазой после интерферонов): заблокировать синтез вирусных белков, распознать вирус, слепить/связать в удобные для транспортировки комки, доставить в лимфоузлы, а также позвать побольше клеток иммунитета в зону «военных действий» — первую локацию инфекции в организме. После этого в ближайших лимфоузлах при распознавании вирусных белков начинается фаза ответа адаптивного иммунитета, специфичного для конкретного вируса. Цели этой, третьей, фазы:
- настроить иммунный ответ с общей непонятной паники на противовирусный ответ (выбрать и активировать нужные клетки Т-хелперы);
- выбрать из разнообразия Т-клеток те, которые способны убить зараженные вирусом клетки, не повредив соседние клетки лёгких (активировать Т-киллеры);
- дополнительно выработать антитела с помощью В-клеток, чтобы блокировать готовые вирусные частицы.
Реакция адаптивного иммунитета точнее и безопаснее, на этой фазе организм стремится уменьшить мощности врождённого иммунитета и быстро ответить с помощью адаптивных иммунных клеток. Если нашлись специфичные к вирусу Т-клетки и В-клетки (способные узнать белковые фрагменты вируса своими Т- и В-клеточными рецепторами), они получают лицензию на работу и размножение, это значит, что в организме формируется клон клеток — множество одинаковых специфичных к вирусу клеток. Из этого множества одинаковых потомков часть клеток скорее всего выживет и сформирует иммунную память, чтобы повторно человек не заразился.
Самая важная часть противовирусного адаптивного иммунного ответа — это специфичные Т-киллеры (CD8+ Т-клетки), которые уничтожают заражённые клетки респираторного/кишечного эпителия. При этом тоже повреждается ткань альвеол, но иначе мы не можем избавиться от вируса, уютно и спокойно размножающегося внутри наших клеток. Т-клеточный иммунный ответ на новые инфекции сильно ослабляется с возрастом, особенно после 60 лет. Специфичную Т-клетку к совершенно новой инфекции сложно подобрать, скорее всего, у пожилого пациента в организме вообще нет таких подходящих клеток: почти все Т-клетки представляют собой клоны иммунной памяти на старые прошедшие инфекции, а тимус (вилочковая железа) уже не производит новые Т-клетки [2].
Что делать иммунитету, если не хватает подходящих Т-клеток?
В этот момент макрофаги в лёгких выделяют сигналы, призывающие больше Т-клеток в лёгкие. Однако среди появляющихся не будет специфичных к вирусу клеток, и сигналы воспаления продолжаются и усиливаются. Иммунная система «сходит с ума» и производит сигналы воспаления без остановки, этот процесс называют цитокиновым штормом. Это лихорадка, которая тяжело переносится организмом и может привести к отказу органов; кроме того, накапливается жидкость в лёгких; ткань лёгких повреждается в результате активации макрофагов и нейтрофилов. Многие называют это иммунным парадоксом, свойственным и новому вирусу, и предыдущим коронавирусам SARS (атипичная пневмония) и MERS (ближневосточный респираторный синдром): у пациентов со слабым, подавленным адаптивным иммунитетом в патогенезе развивается сильная реакция врождённого иммунитета — опасный для жизни цитокиновый шторм. Кстати, раннее отслеживание чрезмерного уровня воспаления в крови пациентов и активное подавление цитокинового шторма — одна из стратегий лечения COVID-19. Например, применяются антитела-блокаторы воспалительного цитокина IL-6 (они помогают контролировать воспаление: оно не уменьшается, но перестаёт увеличиваться), тестируются и другие блокаторы факторов воспаления или их рецепторов. Вообще про подходы лечения рекомендую читать здесь: http://spid.center/ru/articles/2678/.
Важны ли антитела [3], которые производят В-клетки, начиная со второй недели инфекции?
Очень многие эксперты сейчас говорят и пишут, что как только ваш организм начинает вырабатывать нейтрализующие коронавирус антитела, вы точно выздоровеете, это дело времени. Это не совсем так. Кроме того, что можно не успеть обогнать вирус, сейчас всё больше данных говорит о том, что антитела усиливают повреждение лёгких и ускоряют кровоизлияние в них, от которого человек погибает. Например, здесь показано, что титр (концентрация, уровень в плазме крови) IgG-антител скоррелирован с возрастом, тяжёлыми симптомами и лимфопенией (снижением количества клеток адаптивного иммунитета). Это же показывает и модель, в которой макак заражали предыдущим вирусом SARS (высокий титр эффективных нейтрализующих антител IgG к spike-белку оболочки коронавируса коррелировал с сильным повреждением ткани лёгких). Почему так происходит, что от антител ухудшается течение COVID-19, интуитивно же должно же быть наоборот?
Дело в том, что кроме последовательности
врождённый иммунитет → доставка вируса или его обломков в лимфоузел → подбор, поиск и активация адаптивного иммунитета
есть и следующая часть: адаптивный иммунитет выбрал стратегию конкретного иммунного ответа (Т-хелперы подумали и решили) → часть оружия врождённого иммунитета выключается, нужная часть продолжает использоваться. Здесь антитела типа IgG1 направляют и активируют конкретную часть врождённого иммунитета: атаку М1-воспалительных макрофагов на клетки, на поверхности которых сидит вирус. Это не сломанная, а адекватная реакция именно на вирусную инфекцию, но чрезмерная. До этого часть макрофагов в лёгких находились в спокойном режиме, в котором они стимулируют регенерацию: размножение клеток, рост матрикса [4], на котором клетки живут; а также занимались уборкой мёртвых клеток и мусора. М1-воспалительные макрофаги уничтожают матрикс, атакуют клетки, облепленные вирусом, и очень быстро разрушают тонкие альвеолы.
Как же тогда сработают терапевтические антитела к коронавирусу?
Возможно, при производстве терапевтических антител подойдёт применяющийся сейчас подход с оптимизацией по максимальной прочности связывания антител с вирусом. При этом может возникнуть необходимость поменять изотип гуманизованных антител, например, с IgG1 на IgG4, т.к. IgG4 будут мешать вирусу проникать в клетку, но не будут активировать макрофаги. Возможно, подход к подбору терапевтических антител придётся поменять и это вообще будет антитело не на spike-гликопротен вируса, а на другой антиген. Относительно лечения пациентов с COVID-19 сывороткой, полученной от переболевших этим заболеванием людей, что-то определённое сказать сложно, т.к. подобный препарат будет содержать смесь антител с разными свойствами и функциями, и прогнозировать результат терапии на современном этапе весьма затруднительно. Об этом проще будет говорить по результатам, которые мы увидим в течение следующих двух-трёх месяцев.
Есть ли у SARS-CoV-2 особенные механизмы подавления иммунитета, неправильной активации иммунитета?
За последние недели я видела довольно много противоречивых данных о лимфопении (снижении количества клеток адаптивного иммунитета) у пациентов COVID-19. Пока непонятно, это все клетки ушли на войну в лёгкие/кишечник и поэтому снижена численность в крови? Или иммунные клетки активно погибают? Вопрос остаётся открытым, но и не все исследования подтверждают этот факт. В некоторых когортах не было разницы по общей численности лимфоидных клеток между пациентами с лёгким и тяжёлым протеканием болезни, то есть лимфопения под вопросом.
Кажется, есть возможность для более сложной регуляции работы В-клеток и выработки антител, но это на данный момент не до конца изучено. В геноме SARS-CoV-2 (у первого SARS такого не было) есть участок, комплементарный продукту гена BLNK, который важен для развития В-лимфоцитов. Теоретически, коронавирус может с помощью этой РНК влиять на дифференцировку новых наивных В-клеток и в селекции активированных В-клеток, пока идёт отбор оптимальных антител, тем самым меняя адаптивный иммунный ответ.
Прививка BCG: проще ли протекает COVID-19 у вакцинированных?
Сейчас есть только нечёткие эпидемиологические данные, и понимание молекулярных механизмов появится нескоро. В целом известно, что БЦЖ снижает частоту тяжёлых осложнений не только в случае туберкулёза, а при различных респираторных инфекциях (особенно если вакцинируют в юном возрасте, по-видимому). Этот положительный эффект обусловлен не специфичным адаптивным иммунитетом, а зависит от феномена «тренированного врождённого иммунитета» и работы иммунных клеток, занимающих промежуточное положение между врождённым и адаптивным иммунитетом. Другими словами, выигрыш, заключающийся в уменьшении частоты осложнений, объясняется через «тренированное» состояние иммунных клеток, живущих в респираторном эпителии. Если преимущество вакцинации БЦЖ подтвердится и для нового коронавируса, то это не будет чем-то удивительным.
P.S. Пруфы по каждому предложению, на чём я основываюсь, и ссылки, где почитать дальше — по запросу, спрашивайте. Про терапию рекомендую читать тут: http://spid.center/ru/articles/2678/. Для вдохновения и мысленных споров использовала https://elemental.medium.com/this-is-how-your-immune-system-reacts-to-coronavirus-cbf5271e530e и свою вирусологическо-иммунологическую ленту твиттера, например, https://twitter.com/VirusesImmunity/status/1243997325804142593.
Что почитать про упомянутые механизмы иммунитета
- Про врождённый иммунитет немного написано здесь: https://biomolecula.ru/articles/immunologicheskaia-nobelevskaia-premiia-2011.
- Больше про то, как тимус генерирует Т-клетки, распознающие разные инфекции, и про старение тимуса, можно прочитать по ссылкам https://biomolecula.ru/articles/naivnye-t-kletki-kliuch-k-dolgoletiiu и https://biomolecula.ru/articles/analiz-individualnykh-repertuarov-t-kletochnykh-retseptorov.
- Хорошие статьи про антитела в иммунитете и про антитела как лекарства: https://biomolecula.ru/articles/antitelo-luchshii-sposob-raspoznat-chuzhogo, https://biomolecula.ru/articles/biotekhnologiia-antitel; https://biomolecula.ru/articles/razrabotka-vaktsin-chem-i-kak-imitirovat-bolezn.
- Про матрикс, на котором живут и растут клетки: https://biomolecula.ru/articles/chto-takoe-vnekletochnyi-matriks-i-pochemu-ego-vse-izuchaiut.
Материал подготовлен по заказу и при участии канала «Рационально о коронавирусе».
Источник Софья Касацкая
Возможно, иммунный ответ на коронавирусную инфекцию уникален
Наше представление о том, как действует, заражая организм, коронавирус SARS-CoV-2, вызвавший пандемию COVID-19, становится всё более ясным, и здесь не обошлось без сюрпризов. Об этом, в частности, — новая статья в Cell (вот рецензия на неё в Stat).
Последовательность нуклеотидов РНК вируса SARS-CoV-2, естественно, уже прекрасно нами изучена, и это позволяет отслеживать мутации и точно определять, какие белки вынуждена вырабатывать клетка, когда вирус овладел соответствующим клеточным механизмом. Вышеуказанная статья информирует о некоторых из этих белков, а вот ещё одна, более ранняя, где упоминаются способные взаимодействовать с ними лекарства. В целом этих вирусных белков немного, ибо все вирусы весьма примитивные, урезанные до минимума организмы. Вспомним, что они начинают с форсирования экспрессии длинного полипептида. Тот (с помощью захваченных клеточных белков) расщепляет себя на множество фрагментов, каждый из которых содержит всё, что необходимо для вируса. Это — пугающе компактный и эффективный «автозагрузочный» механизм. Поскольку вирусных белков мало, каждому из них обычно отводится строго определённая и необходимая функция (возможно, не одна) — очень похоже на то, как работает крохотный стартап! Нет помощников вице-президента, ответственных в вирусном геноме за упрощение методов планирования; вирусы тощие и цепкие.
А это значит, что они представляют собой совершеннейшие образцы эволюции в действии. Вспомним, что главный принцип эволюции — «Всё, что работает». Именно такой у неё смысл, и в чистом виде его способны демонстрировать только вирусы — самые крохотные и стремительно размножающиеся организмы. Вы знаете старую байку, согласно которой дуб — всего лишь средство для жёлудя произвести много желудей? Вирусы живут этим: единственное, что они делают, — это производят много вирусов. Им не нужно осложнять дело вопросами питания, ибо они не едят. Таким образом, они не претерпевают никаких изменений, связанных с метаболизмом, ибо у них нет никакого метаболизма. Им не знакомы безумства, обусловленные половым отбором, ибо они не спариваются. Они заражают клетки и производят много вирусов — вот и всё. И они делают это очень быстро, снова и снова. Любое изменение, которое хотя бы чуть-чуть помогает заражать клетки и создавать добавочное количество вирусных частичек, способных создавать ещё больше вирусных частичек, усиливается, а любое изменение, которое хотя бы едва уловимо действует в противоположном направлении, подавляется.
Данная статья посвящена жизненно важному для этого вирусного бизнеса аспекту: работе с иммунной защитой заражаемых вирусами организмов. Вспомним, что иммунная система человека имеет, в широком смысле, две ветви. У нас есть, во-первых, приобретённая (адаптивная) подсистема, которая активирует специфические нейтрализующие антитела и направляет Т-клетки на очаг инфекции. Эта реакция требует времени; надо многое подвергнуть анализу, прежде чем пустить в ход весь арсенал средств противодействия инфекции. И, во-вторых, у нас есть находящаяся «в постоянной боевой готовности» врождённая иммунная подсистема, которая распознаёт ряд главных признаков инфекции и готова действовать немедленно. Если у неё есть возможность самостоятельно вылечить инфекцию, она, конечно, делает это — в противном случае она как бы держит линию фронта, пока адаптивная иммунная система подводит артиллерию, чтобы начать обстрел.
Что касается вирусов, то для врождённой иммунной системы странные РНК в основном выступают как признак заражения — им не следует плавать вокруг, и, едва такие объекты появляются, срабатывает сигнал тревоги. Улавливающие эти объекты рецепторы (такие как толл-подобные рецепторы, TLR) резко активизируют некоторые транскрипционные факторы, а именно NF-κB и различные регуляторные факторы интерферонов (IRF). Действуя на уровне ДНК, они изменяют транскрипционную активность, что также вызывает множество последствий: например, запускается производство белков-интерферонов типов I и III (в зависимости от типа клеток), которые, в свою очередь, индуцируют выработку ещё целого ряда интерферон-стимулированных генов. Так как их известно более трёхсот, перечислить все эти эффекты — чрезвычайно трудная задача. Не удивительно, что она представляет собой обычную иммунологическую проблему. Секреция указанных интерферонов может осуществляться для предупреждения соседних клеток. Кроме того, производится целый ряд хемокинов, выделяемых для рекрутирования различных типов циркулирующих лейкоцитов.
Вирусы, воздействующие на организмы с такой защитой (в частности, на наш), подвергались и продолжают подвергаться жёсткому давлению естественного отбора, поэтому в настоящее время мы фиксируем опасные патогены, которые, несмотря на селекционный прессинг, всё же находят способы инфицировать нас. Список предпринимаемых вирусами контрмер очень длинный — эти контрмеры вырабатывались веками, — и вот статья, в которой подробно описаны десять наиболее распространённых. Большинство из них сводится к тому, чтобы как можно дольше скрывать вирус от клеточных рецепторов, а также к блокировке их и их нижестоящих партнёров специфическими вирусными продуктами. В данной статье отмечено, что это своего рода гонка вооружений, и у неё есть свои границы. Иммунную систему вроде нашей, разнообразную и способную немедленно уничтожить любой чужеродный патоген, трудно держать в узде; отсюда — масса проблем с аутоиммунными заболеваниями в их нынешнем виде. И патоген, который, прорвав защиту своего хозяина, начинает бешено работать, вполне может сразу же поплатиться за это смертью и лишить себя возможности распространяться. Успешные патогены (мы говорим об успехе с их точки зрения) умудряются распространяться так, что всегда остаются возможности для роста.
В данной новой статье проведено сравнение транскрипционных изменений, возникающих при заражении, с одной стороны, нынешним коронавирусом, а с другой — ранее выявленными коронавирусами SARS и MERS, а также некоторыми некоронными респираторными вирусами. И оказалось, что SARS-CoV-2 специфичен: ему удаётся весьма эффективно блокировать иммунную реакцию с участием интерферонов типов I и III, одновременно вызывая аномально высокую секрецию цитокинов. Такого профиля не обнаружено ни у одного из других исследованных вирусов. Снова добавив IFN-I в заражённые клетки клеточной культуры, вы увидите, что вирус быстро исчезает — механизм работает, просто он не задействован. Аналогичная картина с общим транскрипционным профилем SARS-CoV-2 в клетках: он уникален. Нельзя сказать, что этот вирус вызывает больше изменений; фактически, транскрипционных различий меньше, чем в случае с другими вирусами, взятыми для сравнения. Но паттерн генов, подвергшихся воздействию, — новый. Несомненно, что имеет место множество вариантов экспрессии целого списка хемокинов: CCL20, CXCL1, IL-1B, IL-6, CXCL3, CXCL5, CXCL6, CXCL2, CXCL16 и TNF.
Эти результаты исследования клеточной культуры довольно хорошо коррелируют с результатами исследования модельных животных (в данном случае хорьков). Наблюдая в течение длительного времени инфицированные клетки назального эпителия данных животных, учёные зафиксировали тот же дефицит интерферонной реакции и ту же усиленную секрецию цитокинов вкупе с, как написано в отчёте,
«уникальной сигнатурой экспрессии генов, обогащённой гибелью клеток и активацией лейкоцитов».
По сравнению с тем, что наблюдалось у хорька при его инфицировании вирусом гриппа А, транскрипционный ответ на коронавирус оказался гораздо менее драматичным, но очень своеобразным. Команде исследователей даже удалось проверить, как идёт транскрипция в лёгочной ткани человека (проведено сравнение 2 образцов, взятых после смерти больных, с 2 образцами, взятыми у здоровых людей). Это очень маленькая выборка, сделать её больше не было возможности, но зафиксированный профиль оказался очень похожим: отсутствие активации интерферонов и усиленная транскрипция цитокинов. Учёные всё же сумели проверить соответствующие уровни циркуляции на большем количестве пациентов (24 инфицированных и контрольная группа из 24 неинфицированных). И здесь получена высокая корреляция с более ранними результатами: отсутствие интерферонного ответа, но рост уровня хемокинов CXCL9 (привлекает Т-клетки), CXCL16 (привлекает NK-клетки), CCL8 и CCL2 (рекрутируют моноциты и/или макрофаги) и CXCL8 (привлекает нейтрофилы). Внезапно возникающий избыток этих типов клеток может быть причиной патологии заболевания, которую, если гипотезы учёных подтвердятся, можно охарактеризовать как однозначно несбалансированный ответ: слишком мало интерферонов и слишком много цитокинов, причём преждевременно.
Я ожидаю публикации целого ряда других статей на данную тему; посмотрим, не изменится ли картина. Но она, безусловно, соответствует тому, что наблюдается в клинических условиях, и предвещает хорошее будущее методам лечения, направленным на ослабление путей цитокиновой реакции. Означает ли это, что введение IFN-I или IFN-III также окажется полезным?
Оригинал Дерек Лоу
Перевод Александр Горлов
COVID-19 может оказаться сосудистым, а не респираторным заболеванием
Многие из странных симптомов коронавирусной болезни имеют одну общую черту.
ВНИМАНИЕ! Научная публикация, на которую опирается последняя часть этой статьи, отозвана, так как не всем авторам работы был предоставлен доступ к исходным данным, также эти данные не были предоставлены для стороннего аудита. Авторы признают, что не могут подтвердить правдоподобность данных и требуют, чтобы статья была отозвана.Что это за данные?
Авторы использовали базы наблюдений из 169 больниц в разных частях света — Азии, Европе и Северной Америке — и по ним оценивали взаимосвязь сердечно-сосудистых заболеваний со смертностью. Использовались больничные данные о пациентах, которые были госпитализированы в период с 20 декабря 2019 года по 15 марта и зарегистрированы в реестре Surgical Outcomes Collaborative как умершие или выжившие по состоянию на 28 марта 2020 года.
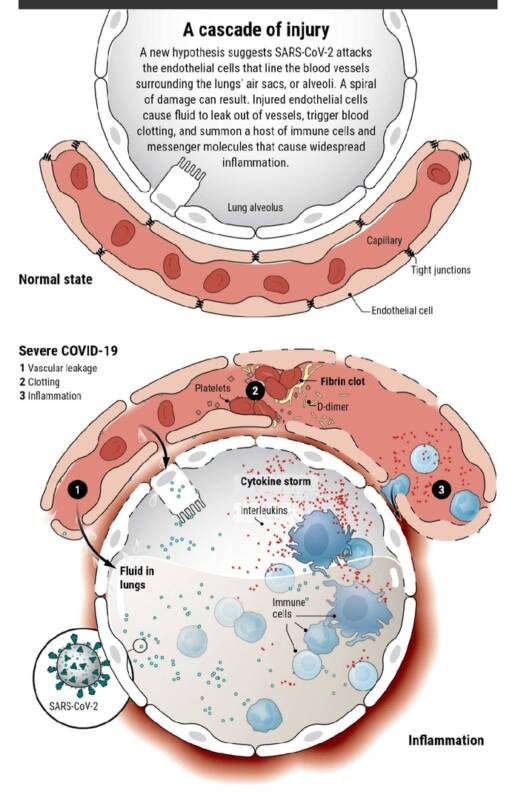
Одним из загадочных симптомов COVID-19, на который обратили внимание в апреле, стал тромбоз. Раньше предполагали, что новый коронавирус в основном поражает лёгкие и вызывает пневмонию. Но довольно быстро стали поступать сведения, что молодые люди с коронавирусом умирают от одного определённого осложнения, от инсульта. Затем стало известно, что у больных присутствует симптом «ковидных» пальцев ног, которые краснеют и приобретают фиолетовый оттенок.
Что общего у таких симптомов? Все они вызваны нарушением кровообращения. Плюс к тому, 40% смертей от COVID-19 вызваны осложнениями на сердце. Инфекция начинает казаться уже скорее сердечно-сосудистой, а не просто респираторной.
Спустя несколько месяцев после начала пандемии начал формироваться корпус доказательств в пользу того, что новый коронавирус может инфицировать сосуды. А это, в свою очередь, может объяснить не только высокую распространённость тромбоза, инсультов и инфарктов, но и разнообразные симптомы, проявляющиеся, буквально, с головы до ног.
Уильям Ли (William Li), президент Фонда ангиогенеза (Angiogenesis Foundation) и врач по профессии, рассказывает:
«Тромбоз, повреждение почек, воспаление сердца, инсульты, отёчность мозга — все эти коронавирусные осложнения были для нас загадкой. Мы столкнулись с целым рядом симптомов, которых нет ни при SARS, ни при H1N1. Если честно, их не наблюдается при большинстве других инфекционных заболеваний. Но тогда казалось, что эти симптомы не связаны между собой».
Если свести все данные воедино, окажется, что этот вирус — кардиоваскулярный, что он влияет на сосуды. Так считает Мандип Мехра (Mandeep Mehra), медицинский директор Сердечно-сосудистого центра Больницы «Бригем-энд-Уименс» (Brigham and Women’s Hospital), врач по профессии.
В статье, опубликованной в апреле в научном журнале The Lancet, Мехра и коллеги доказывают, что вирус SARS-CoV-2 может инфицировать клетки эндотелия, которые выстилают сосуды и защищают кровеносную систему от повреждений. Они синтезируют белки, влияющие на все процессы системы от свёртывания крови до иммунного ответа. В статье учёные показали, что у коронавирусных больных наблюдается повреждение эндотелиальных клеток в лёгких, сердце, почках, печени и кишечнике.
«Зарождается мнение, что COVID-19 — это не только респираторное заболевание, а в первую очередь заболевание кровеносной системы, которое убивает людей, повреждая сердечно-сосудистую систему, но сначала проявляет себя как респираторное»,
Уникальный респираторный вирус
Насколько нам известно, SARS-CoV-2 проникает в тело человека через рецепторы ангиотензинпревращающего фермента (АПФ2), располагающиеся на поверхности клеток, выстилающих дыхательные пути в горле и носу. Скорее всего, как только вирус оказывается в лёгких, он перемещается из альвеол в кровеносные сосуды. А они тоже богаты рецепторами АПФ2.
«[Вирус] проникает в лёгкие и разрушает ткани. Как следствие, люди начинают кашлять. Из-за разрушений, некоторые капилляры разрываются, и вирус начинает инфицировать клетки эндотелия одну за другой. Это вызывает локальный иммунный ответ и воспаление»,
Респираторный вирус, заражающий клетки крови и циркулирующий по организму, — это что-то доселе неслыханное. Среди вирусов гриппа, таких как H1N1, так не ведёт себя ни один, а вирус SARS, родственный возбудителю текущей инфекции, не распространяется в другие ткани организма через лёгкие. Вирусы других типов, повреждающие клетки эндотелия, например Эбола или лихорадка Денге, вообще не похожи на вирусы, обычно поражающие лёгкие.
Бенхур Ли (Benhur Lee), профессор микробиологии на Факультете медицины Икана Медицинского центра Маунт-Синай (Icahn School of Medicine at Mount Sinai) и врач по профессии, говорит, что разница между SARS и SARS-CoV-2 пролегает в присутствии у первого вируса дополнительного белка, необходимого для активации и распространения. Хотя оба вируса прикрепляются к клеткам через рецепторы АПФ2, вирусу SARS необходим ещё один белок, чтобы переместить свой генетический материал в заражаемую клетку, и он есть только у клеток лёгочной ткани. В отличие от этого, белок, нужный для активации SARS-CoV-2, присутствует во всех клетках, в том числе и в клетках эндотелия.
«Белок, необходимый для расщепления SARS, вероятно, присутствует только в лёгких, поэтому там вирус и размножается. Насколько мне известно, он не распространяется на весь организм. [SARS-CoV-2] расщепляется белком под названием фурин, а фурин присутствует во всех человеческих клетках, поэтому вирус представляет большую опасность»,
Странные симптомы вируса можно объяснить повреждением эндотелия
Предположение, что мы имеем дело с инфекцией сосудов, проливает свет на многие странности коронавируса, например, на частоту такого симптома как тромбоз. Клетки эндотелия выделяют белки, включающие и выключающие систему свёртывания крови. Таким образом они играют важную роль в образовании тромбов. Эти клетки также нужны, чтобы поток крови был «гладким» и зацеплялся за неровности сосудов.
Санджум Сетхи (Sanjum Sethi), интервенционный кардиолог в Медицинском центре Колумбийского университета в Ирвинге (Columbia University Irving Medical Center), рассказывает:
«Клеточный слой эндотелия частично отвечает за контроль тромбоза, он ингибирует образование кровяных сгустков различными способами. Если он подвержен повреждению, то можно понять, почему происходит формирование тромбов».
Повреждение эндотелия может оказаться причиной высокой частоты повреждений сосудов и внезапных сердечных приступов у людей с COVID-19. Повреждение эндотелия приводит к воспалению в сосудах, а это, в свою очередь, может привести к отрыву тромба, чего вполне достаточно для того, чтобы получить инфаркт. Это означает, что у любого, у кого в сосудах есть тромб, который обычно находится в стабилизированном положении или под медикаментозным контролем, внезапно возрастает риск сердечного приступа.
«Воспаленный и выведенный из строя эндотелий способствуют отрыву бляшки. Эндотелиальная дисфункция связана с ухудшением прогноза по заболеваниям кровеносной системы, в том числе по инфаркту миокарда»,
Повреждение кровеносных сосудов также может объяснить, почему люди с хроническими заболеваниями, как то повышенное артериальное давление, высокий уровень холестерина, диабет или болезни сердца, подвергаются большему риску серьёзных осложнений от «респираторного» вируса. Все заболевания из перечисленных вызывают дисфункцию эндотелиальных клеток. Будучи усугублёнными повреждением эндотелия и воспалением сосудов, вызванными коронаирусом, эти хронические заболевания обостряются и могут привести к серьёзным проблемам.
Такая теория может даже помочь ответить на вопрос, почему искусственной вентиляции лёгких многим пациентам с COVID-19 оказывается недостаточно для облегчения дыхания. Аппараты ИВЛ помогают доставить воздух в лёгкие, но это только одна часть задачи. Для обеспечения кислородом организма настолько же важен и газообмен, проходящий в крови. А этот процесс зависит от функционирования кровеносных сосудов в лёгких.
«Если в сосудах, задействованных в цикле газообмена, есть сгустки крови, то даже если вы искусственно наполняете лёгкие воздухом и потом его откачиваете, при затруднённом газообмене не удастся получить все преимущества от механической вентиляции лёгких».
В статье, опубликованной 21 мая в Медицинском журнале Новой Англии (New England Journal of Medicine), соавтором которой является Уильям Ли, учёные выявили, что у людей, умерших от COVID-19, был широко распространён тромбоз. Кроме этого, инфекция распространилась и на клетки лёгочного эндотелия. Такого не наблюдалось у умерших от H1N1 — у них было в девять раз меньше сгустков крови в лёгких. Даже структура сосудов и капилляров в легких пациентов, умерших от COVID-19, была иной. У тех было гораздо больше новых ответвлений, которые, вероятно, образовались после повреждения исходных кровеносных сосудов.
«Сгустки крови были повсюду. Мы видели, что клетки эндотелия заполнены вирусными частицами, как автоматы по продаже жевательных резинок. Клетки эндотелия набухают, клеточная мембрана разрушается, и вот у вас есть слой поврежденного эндотелия!»
Наконец, может быть, инфицируя сосуды, вирус распространяется по всему организму и заражает другие органы — что очень нетипично для респираторных заболеваний.
«Клетки эндотелия пронизывают всю систему кровообращения с головы до ног, все 100 000 километров кровеносных сосудов по всему телу выстланы этой тканью. Может быть, именно так COVID-19 получает способность воздействовать на мозг и сердце, вызывать покраснение пальцев ног? Распространяется ли вирус SARS-CoV-2 через эндотелиальные клетки или попадает ли через них в кровоток? Пока ответа на эти вопросы нет».
Если COVID-19 — это сердечно-сосудистое заболевание, то лучшая терапия против вируса — не противовирусная
Согласно другой теории, свёртывание крови, как и проявление симптомов в других органах, происходит из-за сильного воспаления вследствие чрезмерного иммунного ответа — так называемого цитокинового шторма. Эта воспалительная реакция может возникать и при других респираторных заболеваниях или при тяжёлых случаях пневмонии, поэтому первые сообщения о тромбах, осложнениях на сердце и неврологических симптомах не вызвали подозрений. Однако масштабность симптомов, наблюдаемых у пациентов с COVID-19, выходит за рамки возможного при воспалениях, наблюдаемых при других респираторных инфекциях.
«Думаю, при заболеваниях, вызванных другими вирусами, также существует повышенная вероятность свёртывания крови. Этому способствует воспаление в целом. Имеем ли мы при SARS-CoV-2 дело с чем-то большим, или это просто следствие гораздо более сильной инфекции? Это очень важные вопросы, на которые, к сожалению, у нас пока нет ответа»,
Как ни странно, число обращений, которые поступили группе реагирования на лёгочную эмболию (то есть, тромбы в лёгких), которой заведует Сетхи, в апреле 2020 года оказалось в 2—3 раза больше, чем в апреле 2019 года. Сейчас он пытается понять, произошло ли это из-за того, что в апреле этого года в его больнице было просто больше пациентов в связи с пандемией, или потому, что у пациентов с COVID-19 действительно повышенный риск образования тромбов.
«Исходя из того, что я вижу как на практике, так и на предварительных данных, я предполагаю, что заражение этим вирусом повышает риск развития тромбоза, но пока не могу доказать это».
Есть и луч света в тёмном царстве: если COVID-19 является заболеванием кровеносной системы, то существуют готовые лекарства, которые могут помочь защитить пациентов от повреждения эндотелиальных клеток. В другой статье из Медицинского журнала Новой Англии Мехра и коллеги рассмотрели почти 9000 человек с COVID-19 и показали, что использование статинов и ингибиторов АПФ было связано с более высокими показателями выживаемости. Статины снижают риск сердечных приступов не только за счёт снижения уровня холестерина или предотвращения образования тромбов, они также стабилизируют уже наличествующие тромбы. А это значит, что при таких условиях у тромбов меньше шансов оторваться.
«Оказывается, и статины, и ингибиторы АПФ чрезвычайно эффективно защищают от сосудистой дисфункции. Большая их польза в противодействии целому ряду сердечно-сосудистых заболеваний — будь то повышенное артериальное давление, инсульт, инфаркт, аритмия или сердечная недостаточность — обусловлена тем, что они стабилизируют клетки эндотелия»,
По словам Мехры, возможно, лучшая противовирусная терапия на самом деле не является противовирусной. Лучшей терапией может оказаться лекарство, которое стабилизирует сосудистый эндотелий. Учёные пытаются проверить и развить эту концепцию.
Источник XX2 век
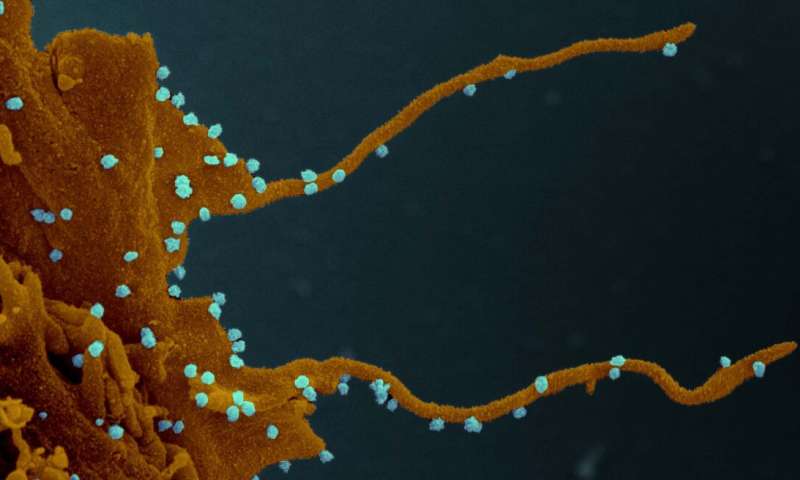
«Патоген влияет и на внешний вид клеток, что показывает последнее исследование, опубликованное в журнале Cell. Они становятся длинными и разветвленными, что способствует распространению инфекции.
«Отчетливая визуализация обширного ветвления филоподии еще раз проясняет, как понимание биологии взаимодействия вируса и хозяина может осветить возможные точки вмешательства в болезнь»
— говорит Неван Кроган, директор Института количественных биологических наук в UCSF и старший исследователь в институте Гладстона».
Источник naked-science