Научный прогресс дал человечеству эффективную медицину и комфортные условия обитания, благодаря которым люди стали жить дольше. Но вместе с этим «химическая революция», начавшаяся в 30-х годах прошлого века, привела к совершенно невиданным результатам. В биосферу Земли стали попадать вещества, синтезируемые человеком для своих нужд, которые действовали неожиданным и плохо понятным образом. Так как они не убивали сразу, подобно сильным отравляющим веществам, а действовали отсроченно, спустя годы и даже поколения, ученые не сразу поняли, с чем они имеют дело. Это было похоже на расследование настоящей детективной истории. Накапливаясь в живой природе, а затем и в организмах людей, эти химикаты дают гормоноподобные эффекты (рис. 1). Часто их воздействие имеет эпигенетический, трансгенерационный характер, наследуемый следующими поколениями. И наиболее уязвимыми к действию этих веществ оказались дети во время внутриутробного развития и в первые годы жизни. Что же это за вещества?
![Рисунок 1. Эндокринные разрушители. Сверху, по часовой стрелке: диоксины, фталаты, огнезащитные средства, фенолы, полихлорированные бифенилы (ПХБ), пестициды, полиароматические углеводороды, фитоэстрогены. Источник [1]](http://www.socialcompas.com/wp-content/uploads/2020/04/01.endokrinnye-razrushiteli.png)
Рисунок 1. Эндокринные разрушители. Сверху, по часовой стрелке: диоксины, фталаты, огнезащитные средства, фенолы, полихлорированные бифенилы (ПХБ), пестициды, полиароматические углеводороды, фитоэстрогены.
Источник [1]
Одной из главных причин такого опасного и печального состояния является воздействие на организм различных химикатов, использующихся в промышленности и сельском хозяйстве.
Начало изучения. Экологические катастрофы
Содержание
История изучения эндокринных разрушителей началась во второй половине прошлого века. Одной из первых на проблему пагубно воздействующих на всё живое химических веществ обратила внимание американский биолог Рэйчел Карсон. Эта смелая женщина показала всему миру, на что способен всего один неравнодушный человек. Ее книга «Безмолвная весна», вышедшая в 1962 году, рассказала об экологических бедствиях, вызванных пестицидами, прежде всего ДДТ. Несмотря на яростное сопротивление химических гигантов, Monsanto и DuPont, бурная реакция общественности, возникшая в ответ на книгу Карсон, привела к позитивным изменениям в области защиты природы. Были внесены поправки в законодательство, касающиеся ограничений производства и применения химикатов. И, как итог, первая победа человечества над химическими магнатами — запрет ДДТ, вначале в Швеции, а затем в США и большинстве стран мира. Но это было только началом борьбы.
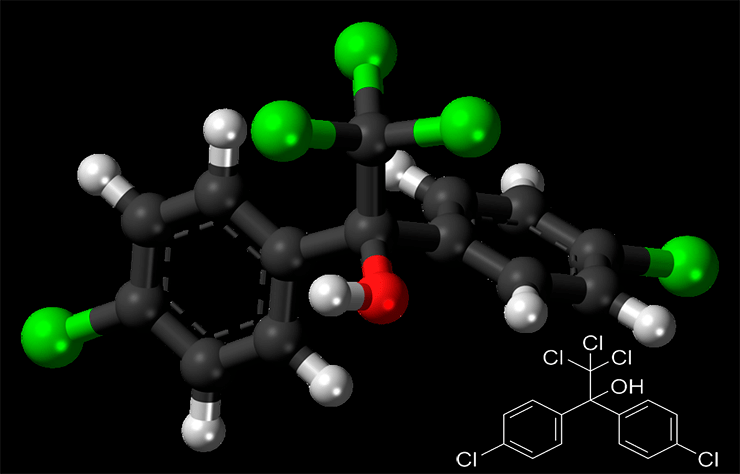
После этого тема эндокринных разрушителей снова оказалась в центре внимания в начале 70-х годов прошлого века, в связи с экологической катастрофой в районе Великих озер (США и Канада). Многолетнее бесконтрольное загрязнение их акватории отходами химических предприятий привело к резкому сокращению количества всех живых организмов в экосистеме: рыб, птиц, земноводных и млекопитающих. Проведенные анализы показали причину такого бедствия. В воде озер обнаружили различные химические соединения, не свойственные живой природе: ДДТ и его метаболит (продукт распада) ДДЭ (дихлордифенилдихлорэтилен), пестициды дильдрин (рис. 2) и мирекс, полихлорированные бифенилы, тяжелые металлы (ртуть, свинец) и другие химикаты [3]. И все они были выявлены в водорослях и животных, обитающих в районе Великих озер. Кроме этого, из-за слива химических отходов ил на дне озер подвергся радиоактивному заражению и содержал большое количество радионуклидов. Все перечисленные вещества нашли и у местного населения, которое активно употребляло в пищу животных.
Проведенные исследования показали, что стало причиной сокращения численности представителей водной фауны Великих озер: нарушения в репродуктивной системе. У рыб наблюдалось замедленное формирование органов репродуктивной системы, снижение уровня тестостерона, гидроксипрогестерона и эстрадиола, уменьшение размеров гонад и плохая выраженность (или отсутствие) вторичных половых признаков. В целом физиологические различия между полами стирались: самки становились похожими на самцов, а самцы — на самок. Это не давало возможности рыбам нормально размножаться.
Ученые наконец занялись этим вопросом всерьез, и оказалось, что люди и животные подвергаются большой и малоизученной опасности. Выяснилось, что среди химикатов, которые используются в промышленности и сельском хозяйстве и в больших количествах попадают в водоемы и почву (а потом в продукты питания), очень много веществ, в значительной степени влияющих на внутренние биологические процессы. Из-за своего характерного механизма воздействия они были названы эндокринными разрушителями.
Сам термин endocrine-disrupting chemicals ввели в научный оборот в 1993 году американские биологи — Ана Сото и ее коллеги [4]. Существует несколько трактовок, что же такое эндокринные разрушители. Вот какое определение им дает Агентство по охране окружающей среды США:
-
Эндокринный разрушитель: экзогенный агент, который препятствует синтезу, секреции, транспорту, метаболизму, связывает действие или ликвидирует естественные гормоны в крови, которые несут ответственность за гомеостаз, воспроизводство и процесс развития.
А вот как описывает эндокринных разрушителей ВОЗ [5]:
-
Эндокринный разрушитель:это экзогенное химическое вещество (смесь), которое нарушает функцию эндокринной системы и тем самым вызывает неблагоприятные эффекты в организме человека, или его потомства, или (суб)популяции.
И, пожалуй, наиболее лаконично дало определение эндокринным разрушителям Американское общество эндокринологов:
-
Эндокринный разрушитель: экзогенное [не природное] химическое вещество (или смесь химических веществ), которое влияет на любой аспект действия гормонов.
В русскоязычной научной литературе, кроме термина «эндокринные разрушители», также встречаются и другие, обозначающие данный класс химических веществ: гормоноподобные ксенобиотики (ГПК) и химические вещества, нарушающие работу эндокринной системы (ХВНРЭС).
К ним относят химикаты — полимеры, пластификаторы, диоксины, тяжелые металлы, пестициды, растворители, лекарства, — которые при попадании в организм человека имитируют или блокируют действие определенных гормонов. Это нарушает развитие и нормальное функционирование эндокринной системы организма, работа которой, в свою очередь, тесно связана с репродукцией и размножением (рис. 3) [6]. В первом случае, когда эндокринные разрушители действуют подобно гормонам, они активируют гормональный рецептор, который принимает их за гормон, запуская клеточные процессы, которые обычно активируются только эндогенными гормонами. Во втором случае эндокринные разрушители могут связываться с рецептором и заблокировать его, препятствуя таким образом активации рецептора циркулирующим гормоном.
![Рисунок 3. Модель эндокринных систем, являющихся мишенью эндокринных разрушителей. Их действию подвержены все основные эндокринные органы, в том числе гипоталамо-гипофизарная ось, надпочечники, репродуктивные органы, поджелудочная железа и эпифиз. Источник [6]](http://www.socialcompas.com/wp-content/uploads/2020/04/03.model-endokrinnyh-sistem.png)
Рисунок 3. Модель эндокринных систем, являющихся мишенью эндокринных разрушителей. Их действию подвержены все основные эндокринные органы, в том числе гипоталамо-гипофизарная ось, надпочечники, репродуктивные органы, поджелудочная железа и эпифиз.
Источник [6]
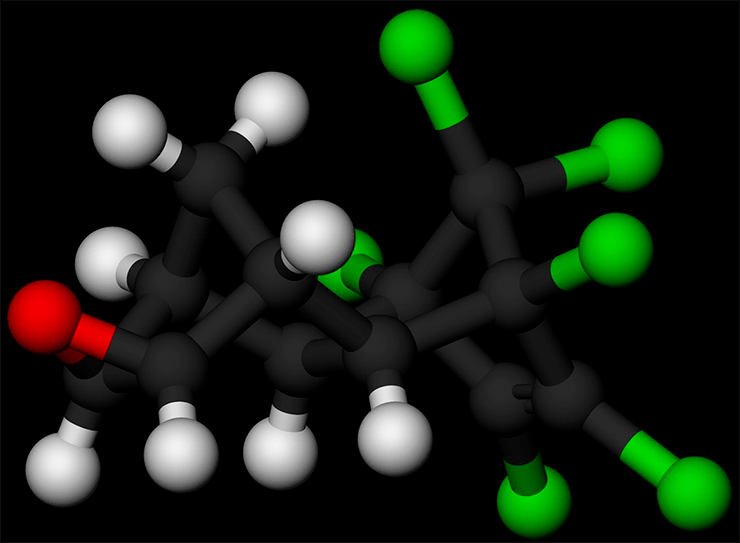
Еще одна крупная экологическая катастрофа, связанная с эндокринными разрушителями, произошла в 1980 году в американском штате Флорида. Из хранилища с химическими токсикантами в озеро Апопка попало большое количество ДДТ, продукта его распада ДДЭ (который в 16 раз биологически активнее ДДТ), пестицида дикофола (рис. 4), хлорбензолата (производного хлорбензола) и дихлорбензофенона. Загрязнение озера этими химикатами привело к тому, что в водоеме почти полностью вымерла популяция аллигаторов. Причиной этому стало антиандрогенное действие попавших в воду химикатов, снижавшее продукцию тестостерона, и как следствие — критическая феминизация самцов. Так, у них наблюдались атрофические изменения семенных канальцев, нарушения сперматогенеза, снижение содержания в крови тестостерона в четыре раза и увеличение концентрации эстрадиола, а также уменьшение размеров половых органов (подробнее о молекулярных механизмах влияния на мужскую репродукцию рассказывает рисунок 5). В организмах самок аллигаторов кроме снижения уровня тестостерона выявили и значительное увеличение содержания эстрадиола, что приводило к поликистозу яичников и бесплодию [8].
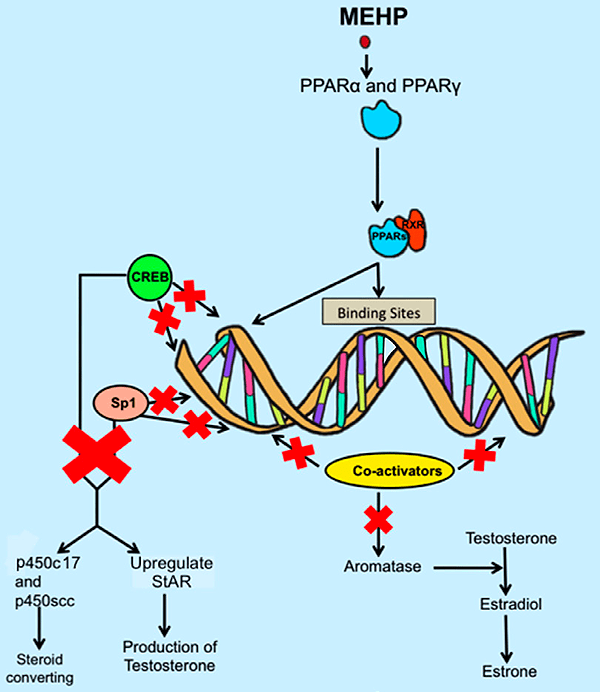
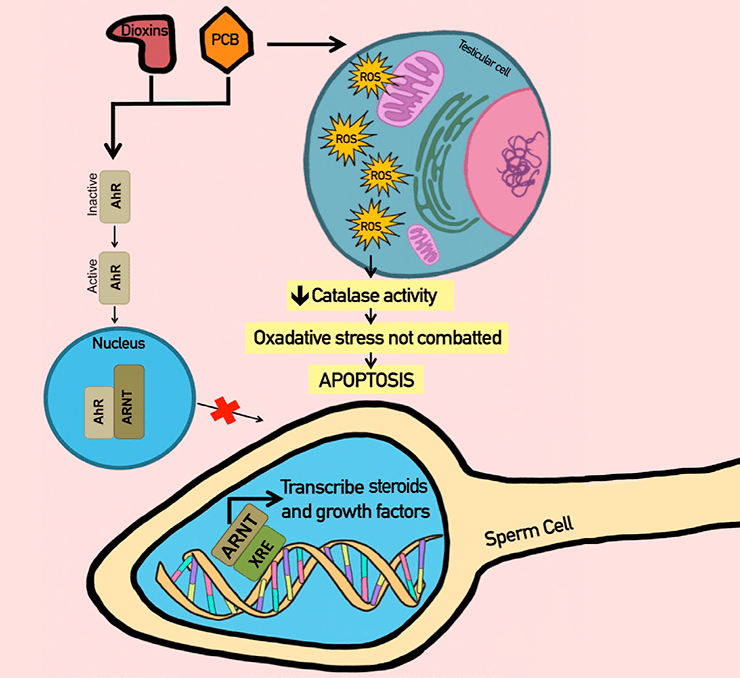
Рисунок 5а. Механизмы действия эндокринных разрушителей на качество спермы. Моно(2-этилгексил)фталат (MEHP) инициирует гетеродимеризацию PPAR, тем самым блокируя сайты связывания ДНК и коактиваторов, необходимые для транскрипции стероид-продуцирующих генов. MEHP — моно(2-этилгексил)фталат; PPAR — рецептор, активированный пролифератором пероксисом. Источник [35]
 Ученые выяснили, что организм особенно чувствителен к действию эндокринных разрушителей во время внутриутробного развития и в первые месяцы после рождения. Примечательно, что этот период совпадает с периодом эпигенетической пластичности (подробнее про эпигенетику см. статью «Эпигенетика: невидимый командир генома» [9]). Во время него организм может «подстраивать» уровень экспрессии своих генов так, чтобы наилучшим образом соответствовать условиям, в которых предстоит жить. «Настройки» же, «сбитые» эндокринными разрушителями в этот период, могут вызвать развитие отклонений в будущем.
Ученые выяснили, что организм особенно чувствителен к действию эндокринных разрушителей во время внутриутробного развития и в первые месяцы после рождения. Примечательно, что этот период совпадает с периодом эпигенетической пластичности (подробнее про эпигенетику см. статью «Эпигенетика: невидимый командир генома» [9]). Во время него организм может «подстраивать» уровень экспрессии своих генов так, чтобы наилучшим образом соответствовать условиям, в которых предстоит жить. «Настройки» же, «сбитые» эндокринными разрушителями в этот период, могут вызвать развитие отклонений в будущем.
Сегодня, после проведенных исследований, считается установленным, что у эндокринных разрушителей нет безопасной пороговой экспозиции — то есть они имеют потенциал оказывать вредное влияние в любом количестве, превышающем значение «ноль». Так, биоцид трибутилтин, который добавляют в корабельную краску для предотвращения обрастания моллюсками, начинал действовать в концентрациях 0,1 нг/л (нанограмм — одна миллиардная часть грамма). Уже в таких дозах он приводил к тому, что у самок брюхоногих моллюсков происходила маскулинизация: наблюдалось появление структур половой системы самцов — сформированных семенных протоков, пениса и др. Это приводило к полной невозможности размножения этих видов. Связаны эти изменения были с тем, что трибутилтин препятствовал эстерификации тестостерона, что вызывало повышение в организме морских животных уровня свободного тестостерона и превращение самок в самцов [10].
Трибутилтин не так давно снова попал в поле зрения исследователей. В 2017 году в Nature Communications вышла статья американских ученых, где они описали действие на организм этого вещества и еще двух эндокринных разрушителей: бутилгидрокситолуола и полимера перфтороктановая кислота. Последняя содержится в посуде, одежде, ковровых покрытиях и питьевой воде и кроме эндокринного разрушителя является ещё и канцерогеном. Указанные вещества вызывали стресс эндоплазматического ретикулума, повреждения митохондрий, ингибировали действие ядерного фактора NF-κB и нарушали функцию «стража генома» — белка р53. Все эти эффекты были зафиксированы в нейроэндокринных клетках мозга и эндокринных клетках кишечника. По мнению ученых, это препятствует нормальному производству и секреции гормонов, контролирующих аппетит, — PYY, α-MSH и CART — и может играть не последнюю роль в современной эпидемии ожирения [11].
Диэтилстильбэстрол
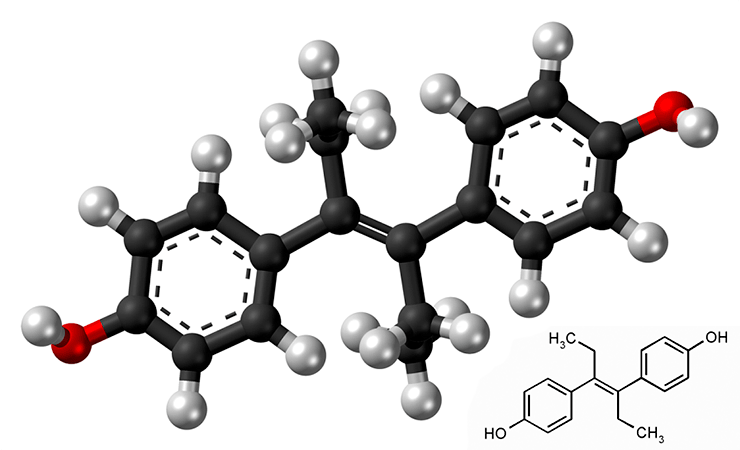
Одним из первых хорошо изученных эндокринных разрушителей стал препарат диэтилстильбэстрол (рис. 6). В 70-х годах прошлого века американский ученый Артур Хербст с коллегами обнаружил взаимосвязь между дородовой терапией диэтилстильбэстролом беременных женщин и развитием опухолей у их дочерей [12]. Диэтилстильбэстрол обладает выраженной эстрогенной активностью, то есть повышает уровень женских половых гормонов. На протяжении 30 лет он активно использовался врачами для лечения некоторых осложнений при беременности. Прозрение пришло после публикации Хербста и его коллег, в которой они показали, что это вещество влияет на программирование патологий у зародыша. Позже их данные подтвердили и расширили другие исследователи.
Диэтилстильбэстрол стал первым известным человеческим трансплацентарным канцерогеном, проникающим через плаценту и оказывающим прямое канцерогенное воздействие на плод. Программируемые эффекты диэтилстильбэстрола могут эпигенетически наследоваться и следующими поколениями. Диэтилстильбэстрол был первым обнаруженным эстрогенным ксенобиотиком, вызывающим деметилирование гена эстрогена и связанную с этим его аномальную экспрессию [13]. У мужчин, чьи матери принимали во время беременности диэтилстильбэстрол, концентрация сперматозоидов была на треть меньше нормы.
Как показали работы Лео Догерти и его коллег из Йельского университета, диэтилстильбэстрол способен влиять на работу гистоновой метилтрансферазы Ezh2, значительно усиливая ее синтез. Такое изменение активности Ezh2, как предполагают ученые, напрямую может быть связано с риском возникновения рака молочной железы [14]. Другая группа исследователей из этого же университета, под руководством Джейсона Бремера, показала, что диэтилстильбэстрол может негативно влиять на уровни метилирования генов Hox, которые относятся к группе так называемых гомеобоксов (последовательностей ДНК, вовлеченных в регуляцию развития у животных). Они отвечают в организме за нормальное развитие эмбриона, в том числе и за развитие женского репродуктивного тракта. Ученые выяснили, что в основе такого негативного влияния диэтилстильбэстрола лежат эпигенетические причины:
«Мы исследовали частоту метилирования ДНК Hoxa10 после внутриутробного воздействия диэтилстильбэстрола и обнаружили аномальное метилирование промотора и интрона Hoxa10 и то, что это измененное метилирование также сохраняется в зрелом возрасте. Кроме того, мы показали, что уровень экспреccии мРНК двух важных ДНК-метилтрансфераз, ферментов, ответственных за метилирование ДНК, повышается. Мы полагаем, что механизм, посредством которого изменяется активность ДНК-метилтрансфераз, включает в себя влияние диэтилстильбэстрола на рецепторы эстрогена» [15].
Пестициды: метоксихлор и винклозолин
Следующими веществами, которые были подробно описаны как эндокринные разрушители, стали пестициды — синтетические хлорорганические инсектициды, широко применявшиеся в сельском хозяйстве для борьбы с вредителями.
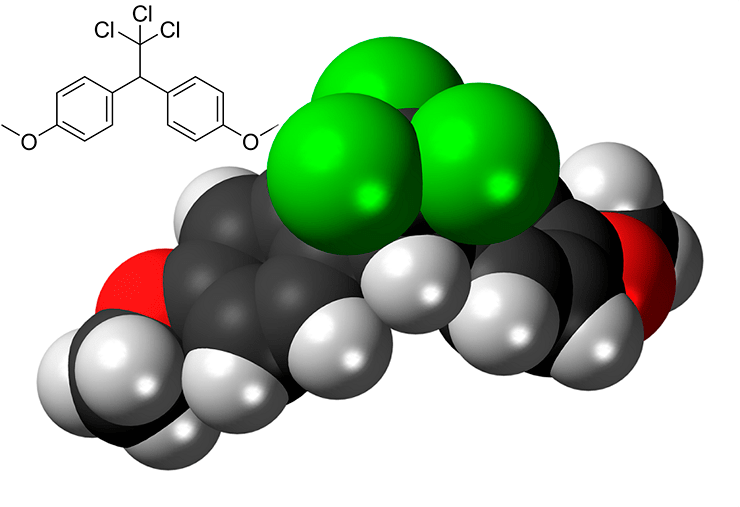
После запрета ДДТ химические компании развернули работу по созданию его эффективных аналогов, одним из которых стал инсектицид метоксихлор (рис. 7).
Но, как оказалось, замена ДДТ вышла не очень подходящей. После проведенных исследований выяснилось, что, попадая в организм с продуктами и водой, метоксихлор может давать целый ряд негативных эффектов.
Среди таких эффектов метоксихлора обнаружили антиэстрогенную и антиандрогенную активности, то есть он мог негативно перенастраивать гормональную систему не только самцов, но и самок. Особенно опасным представляется попадание метоксихлора в организм беременных женщин. На опытах с грызунами выявили целый ряд негативных воздействий этого инсектицида на плод. У беременных крыс, которым в организм попадал метоксихлор, всё потомство рождалось с дефектной репродуктивной функцией. У самок нарушалась функция яичников, у самцов происходило снижение уровня тестостерона и ухудшалось качество спермы. Были обнаружены ярко выраженные эпигенетические изменения под воздействием метоксихлора, например, снижение уровня экспрессии гена эстрогенового рецептора (ER)-beta, вызванное значительным гиперметилированием промоторных регионов этого гена и повышением уровня экспрессии ДНК-метилтрансферазы DNMT3b. Описаны трансгенерационные эффекты метоксихлора, передававшиеся по наследству трем поколениям: изменялось метилирование генов H19, Meg3 (Gtl2), Mest (Peg1), Snrpn и Peg3 в сперматозоидах потомков грызунов, получавших метоксихлор [16].
В 2014 году генетики Ариэн Паолони-Джиакобино и ее коллеги из Женевского университета в ходе исследований обнаружили еще одно негативное свойство метоксихлора. Он отрицательно воздействовал на качество спермы, нарушая один из важных эпигенетических механизмов — геномный импринтинг, происходящий во время развития плода [17].
Не так давно китайские ученые выявили негативное влияние метоксихлора и его метаболитов на ферменты группы цитохрома Р450. Эти ферменты реализуют в организме множество важнейших процессов, связанных с расщеплением и выведением химических веществ, включая лекарственные препараты. Результаты работ китайских биологов показали, что метоксихлор и его метаболиты ингибировали активность системы цитохрома Р450, и это было чревато тяжелыми последствиями [18]. Метоксихлор до сих пор не запрещен и продолжает использоваться, в том числе и в РФ.
Еще одним химикатом, который привлек к себе большое внимание ученых, стал фунгицид винклозолин. В 2005 году профессор биологии Вашингтонского университета Майкл Скиннер c коллегами проводил опыты с беременными мышами, которым добавляли в корм винклозолин. У таких самок потомство мужского пола рождалось с выраженной репродуктивной дисфункцией: самцы имели нарушенный сперматогенез (малое количество и плохое качество сперматозоидов).
Впрочем, такой результат был прогнозируемым в свете других работ, и Скиннер не очень удивился полученным данным. Сюрприз ждал его позже, когда родилось три следующих поколения мышей. Выяснилось, что у всех мышей-самцов наблюдался схожий репродуктивный дефект: нарушение сперматогенеза. Произошло эпигенетическое наследование приобретенных признаков! У самых первых самок, получавших винклозолин, выявили эпигенетическую трансформацию (метилирование ДНК), передававшуюся из поколения в поколение и сошедшую на нет лишь в пятом поколении мышей [19].
Позже обнаружили и другие эффекты винклозолина. Причем, что примечательно: он имеет в основном антиандрогенное действие, то есть вызывает отклонения у представителей мужского пола. Среди таких отклонений, известных сегодня, ученые называют гиперхолестеринемию (повышенный уровень холестерина в крови), болезни почек и простаты, нарушение функций иммунной и репродуктивной систем.
В марте 2015 года Майкл Скиннер опубликовал результаты своих новых исследований, которые показали еще одно негативное воздействие винклозолина. Попадание этого химиката в организм во время беременности нарушало нормальную работу генетического аппарата нервных клеток. И опять в корне нарушений лежали эпигенетические изменения, инициируемые винклозолином [20]. Уже упоминавшаяся выше Ариэн Паолони-Джиакобино описала, как винклозолин, подобно метоксихлору, негативно действовал на геномный импринтинг: воздействие на беременных самок мышей в момент определения пола эмбриона вызывало нарушения в метилировании отцовских и материнских импринтированных генов (H19, Gtl2, peg1, Snrpn и Peg3) в сперматозоидах мужского потомства. Такой эффект сохранялся у трех поколений [16].
Полимеры и пластификаторы
Еще одним классом химических веществ, относящихся к эндокринными разрушителям, являются различные полимеры. Из-за своего удобства и простоты изготовления, полимеры широко используются в различных отраслях промышленности, и их годовое производство исчисляется миллиардами тонн. Один из самых распространенных полимеров — полистирол, из которого, в частности, изготавливается большая часть упаковочного материала (контейнеров, пакетов, бутылок), стаканов, тарелок, а также медицинских изделий. Олигомеры полистирола (дифенилбутан, трифенилгексан, фенилэтилтетралин и др.) имеют свойство мигрировать из упаковочных материалов в продукты. Этот процесс значительно активизируется при нагревании. Как показали исследования, димеры и тримеры стирола оказывают гормоноподобное влияние, связываясь с эстрогенными рецепторами [21].
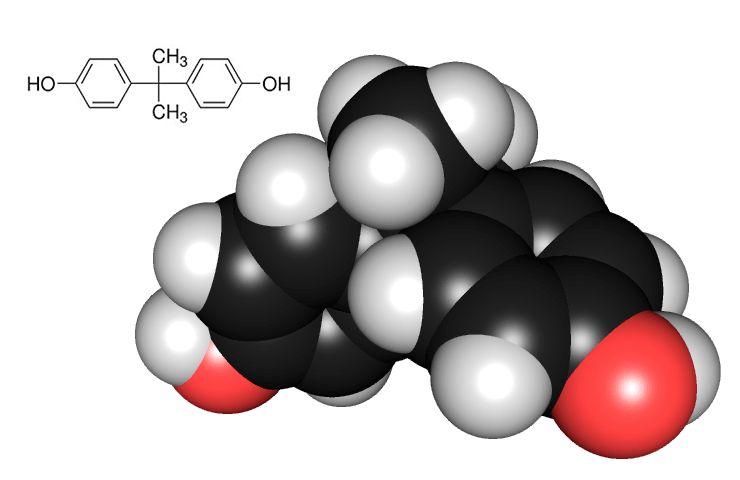
Для придания полимерам характерных эластичных свойств в их состав добавляют различные пластификаторы, фталаты и фенол-стабилизаторы. Эти вещества действуют как эндокринные разрушители, также проникая из упаковочного материала в продукты питания. Самым известным из второй группы (фенол-стабилизаторов) является хорошо изученный сегодня бисфенол А (БФА) (рис. 8). Это вещество очень распространено и окружает нас повсюду. Кроме пластиковых изделий БФА используется в стоматологии (при производстве материалов для пломб) и в консервной промышленности (им выстилают внутреннюю поверхность жестяных консервных банок). Из-за своих характерных свойств (БФА обладает очень сильно выраженной эстрогенной активностью) это вещество еще называют вездесущим ксеноэкстрогеном.
Исследования показывают, насколько широко БФА распространен в окружающем нас мире. По данным, которые приводит в своей работе профессор Первого МГМУ им. И.М. Сеченова Татьяна Романцова, БФА практически постоянно обнаруживается в сыворотке крови человека, а также в грудном молоке и пуповинной крови [22]. В 2003–2004 годах американские исследователи из Центров по контролю и профилактике заболеваний провели масштабный поиск БФА в организмах людей. Из 2500 обследованных у 92% в моче обнаружили БФА, причем концентрации бисфенола были значительно выше в организмах детей и подростков [23]. Это легко объяснимо: детский организм наиболее уязвим для действия токсинов, так как не до конца сформировал защитные системы.
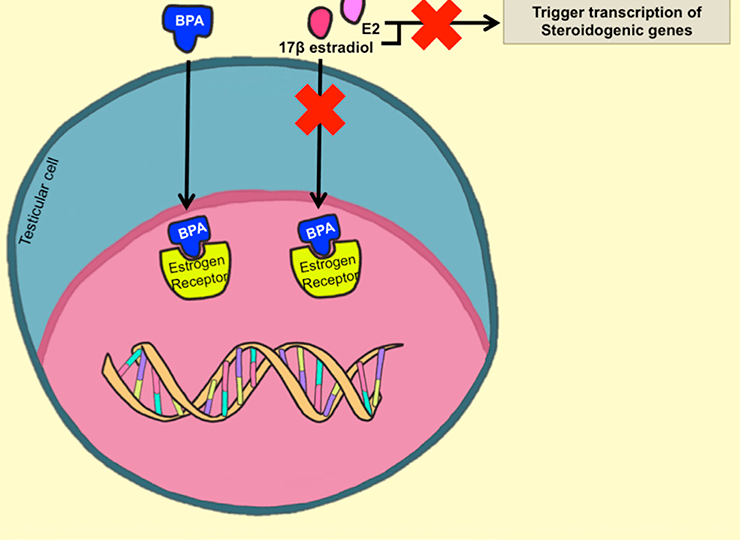
Как показали исследования, БФА способен оказывать ярко выраженное негативное влияние на генетический аппарат яйцеклетки [24]. В период беременности БФА, свободно проникая через плаценту, может накапливаться в тканях плода [25]. Опыты с грызунами показали, что посредством эпигенетических изменений он может негативно влиять на мужское потомство, приводя к феминизации самцов [26]. Кроме этого, попадание БФА в организм плода связывают с развитием во взрослой жизни ряда отклонений, таких как диабет, ожирение и нарушения репродукции [27]. Сводные данные по эффектам эндокринных разрушителей представлены в таблице 1.
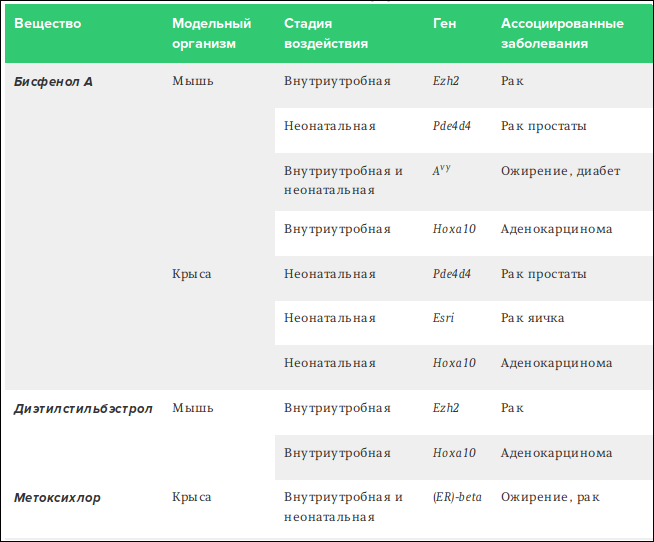 Как и другие эндокринные разрушители, БФА влияет на функционирование организма, избирая в качестве мишеней рецепторы гормонов — эстрогенов, андрогенов, прогестерона, тиреоидных гормонов, а также ядерного рецептора PPAR-γ [16].
Как и другие эндокринные разрушители, БФА влияет на функционирование организма, избирая в качестве мишеней рецепторы гормонов — эстрогенов, андрогенов, прогестерона, тиреоидных гормонов, а также ядерного рецептора PPAR-γ [16].
Кроме БФА, разработали схожий с ним химикат бисфенол С, который должен был заменить БФА как более «безопасный». Но, в итоге, поменяли «шило на мыло»: бисфенол С, который добавляют в пластиковую тару, имеет большое структурное сходство еще с одним эндокринным разрушителем — метаболитом ДДТ, ДДЭ, что обуславливает их сходное воздействие на живые организмы (рис. 9) [28].
![исунок 9. Атомная модель и химическая структура сходных по строению эндокринных разрушителей: бисфенола С (а) и ДДЭ (б) [28]](http://www.socialcompas.com/wp-content/uploads/2020/04/09.DDE-i-bisfenol-C.png)
Рисунок 9. Атомная модель и химическая структура сходных по строению эндокринных разрушителей: бисфенола С (а) и ДДЭ (б)
[28]
Фитоэстрогены
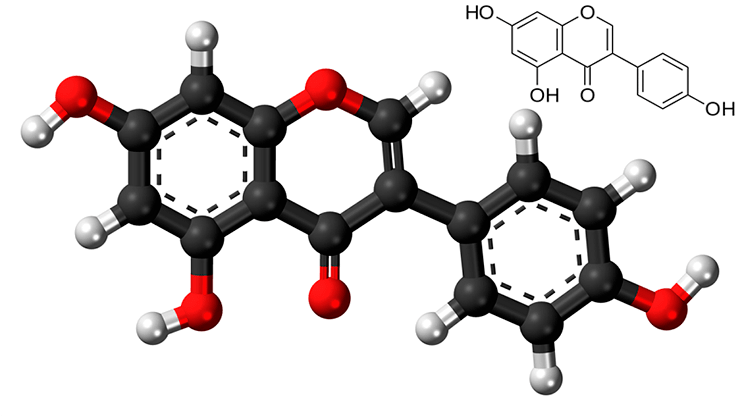
И напоследок упомянем еще об одном классе гормоноподобных веществ, на этот раз природного происхождения — фитоэстрогенах. Они состоят из двух больших групп: изофлавоноидов и лигнанов. Изофлавоноиды изучены лучше, и сегодня описано около 4000 различных их видов. Попадая в кишечник, изофлавоноиды метаболизируются, образуя соединения с гормональными (эстрогенными) свойствами: формононетин, дэйдзеин, генистеин (рис. 10), биоканин А и др. Большое количество изофлавоноидов содержится в сое. С этим ученые связывают меньшую подверженность азиатских женщин, употребляющих соевые продукты, некоторым заболеваниям, в частности раку молочной железы [29].
Удивительная история, связанная с природными гормоноподобными веществами, произошла в середине прошлого века в Австралии. Местные овцы, пасшиеся на пастбищах с клевером Trifolium subterranium, стали болеть «клеверной болезнью». Эта болезнь проявлялась в резком снижении плодовитости овечек. После проведенных исследований ученые выяснили, что в состав клевера входили биофлавоноиды, обладавшие гормоноподобными (эстрогенными) свойствами, которые негативно влияли на репродукцию овец. По мнению некоторых исследователей, клевер в процессе эволюции выработал защитный механизм и так спасался от своего полного уничтожения животными, снижая их численность [30].
Заключение
Мы рассмотрели здесь лишь малую часть веществ-разрушителей, кроме которых есть еще множество промышленных химикатов, действующих сходным образом. В «Национальном докладе о воздействии на человека химических веществ в окружающей среде», подготовленном в феврале 2015 года американскими Центрами по контролю и профилактике заболеваний и Национальным центром по состоянию окружающей среды, перечислены более 200 химических веществ, побочных продуктов технической деятельности человека, представляющих серьезную опасность для экологии и здоровья [31].
Все эти данные говорят нам о том, что наличие эндокринных разрушителей в среде обитания — фактор риска не только для современного человека, но и для будущих поколений. Даже если завтра будет полностью запрещено производство подобных химических веществ, действующих как эндокринные разрушители, на эпигенетическом уровне память о контакте с ними будет сохраняться еще у трех–четырех последующих поколений, совсем не благоприятно сказываясь на их здоровье. А уже накопленные в живой природе вредные химикаты будут разлагаться не одно столетие, отравляя всё вокруг себя. Так, инсектицид ДДТ 30 лет активно использовался во всем мире. Всего этого химиката было произведено более пяти миллионов тонн. Он до сих пор циркулирует в природе, проникая в организмы животных и людей, — и будет циркулировать, по оценкам экологов, как минимум еще столетие [7].
Проблема экологии — это одна из главных наших проблем сегодня, и она касается каждого (об этом писали и на «Биомолекуле» — например, в «А ты такой холодный, как… пластик в океане» [32]). Земной шар слишком мал, чтобы кто-то мог чувствовать себя в безопасности при нынешнем положении дел. Опасные химические вещества не знают границ и обнаруживаются даже там, где никогда не применялись, — в Арктике и Антарктике. Более того, под влиянием еще не до конца выясненных механизмов токсичные химикаты в окружающей среде формируют новые, еще более стойкие к разложению, соединения с высокотоксичными свойствами. Такие, как обнаруженные не так давно соединения трис-4-(хлорфенил)метан (Tris-H) и трис-4-(хлорфенил)метанол (Tris-OH) [33], [34]. Безудержное развитие научно-технического прогресса без учета экологических рисков уже исчерпало себя и должно смениться более разумным и взвешенным подходом к окружающей нас среде.
Литература
- Natalia M. Grindler, Jenifer E. Allsworth, George A. Macones, Kurunthachalam Kannan, Kimberly A. Roehl, Amber R. Cooper. (2015). Persistent Organic Pollutants and Early Menopause in U.S. Women. PLoS ONE. 10, e0116057;
- An estimated 12.6 million deaths each year are attributable to unhealthy environments. (2016). WHO;
- W G Foster. (1995). The reproductive toxicology of Great Lakes contaminants.. Environmental Health Perspectives. 103, 63-69;
- T Colborn, F S vom Saal, A M Soto. (1993). Developmental effects of endocrine-disrupting chemicals in wildlife and humans.. Environmental Health Perspectives. 101, 378-384;
- Global assessment of the state-of-the-science of endocrine disruptors. (2014). WHO;
- Thaddeus T. Schug, Amanda Janesick, Bruce Blumberg, Jerrold J. Heindel. (2011). Endocrine disrupting chemicals and disease susceptibility. The Journal of Steroid Biochemistry and Molecular Biology. 127, 204-215;
- Никитин А.И., Сергеев О.В., Суворов А.Н. Влияние вредных факторов среды на репродуктивную, эндокринную системы и эпигеном. М.: «Акварель», 2016. — 348 с.;
- L J Guillette, T S Gross, G R Masson, J M Matter, H F Percival, A R Woodward. (1994). Developmental abnormalities of the gonad and abnormal sex hormone concentrations in juvenile alligators from contaminated and control lakes in Florida.. Environmental Health Perspectives. 102, 680-688;
- Эпигенетика: невидимый командир генома;
- Meredith P. Gooding, Vickie S. Wilson, Leroy C. Folmar, Dragoslav T. Marcovich, Gerald A. LeBlanc. (2002). The Biocide Tributyltin Reduces the Accumulation of Testosterone as Fatty Acid Esters in the Mud Snail (Ilyanassa obsoleta). Environ Health Perspect. 111, 426-430;
- Uthra Rajamani, Andrew R. Gross, Camille Ocampo, Allen M. Andres, Roberta A. Gottlieb, Dhruv Sareen. (2017). Endocrine disruptors induce perturbations in endoplasmic reticulum and mitochondria of human pluripotent stem cell derivatives. Nat Commun. 8;
- Robboy S.J., Scully R.E., Welch W.R., Herbst A.L. (1977). Intrauterine diethylstilbestrol exposure and its consequences: pathologic characteristics of vaginal adenosis, clear cell adenocarcinoma, and related lesions. Arch. Pathol. Lab. Med. 101, 1–5;
- Li S., Washburn K.A., Moore R., Uno T., Teng C., Newbold R.R., McLachlan J.A., Negishi M. (1997). Developmental exposure to diethylstilbestrol elicits demethylation of estrogen-responsive lactoferrin gene in mouse uterus. Cancer Res. 57, 4356–4359;
- Leo F. Doherty, Jason G. Bromer, Yuping Zhou, Tamir S. Aldad, Hugh S. Taylor. (2010). In Utero Exposure to Diethylstilbestrol (DES) or Bisphenol-A (BPA) Increases EZH2 Expression in the Mammary Gland: An Epigenetic Mechanism Linking Endocrine Disruptors to Breast Cancer. HORM CANC. 1, 146-155;
- Jason G. Bromer, Jie Wu, Yuping Zhou, Hugh S. Taylor. (2009). Hypermethylation of Homeobox A10 byin UteroDiethylstilbestrol Exposure: An Epigenetic Mechanism for Altered Developmental Programming. Endocrinology. 150, 3376-3382;
- . (2014). Early-life Exposure to Endocrine Disrupting Chemicals and Later-life Health Outcomes: An Epigenetic Bridge?. AD;
- Ariane Paoloni-Giacobino. (2014). Epigenetic Effects of Methoxychlor and Vinclozolin on Male Gametes. Vitamins & Hormones. 211-227;
- Bingbing Chen, Peipei Pan, Li Wang, Menchun Chen, Yaoyao Dong, et. al.. (2015). Effects of Methoxychlor and 2,2-bis (p-Hydroxyphenyl)-1,1,1-Trichloroethane on Cytochrome P450 Enzyme Activities in Human and Rat Livers. Pharmacology. 95, 145-153;
- M. D. Anway. (2005). Epigenetic Transgenerational Actions of Endocrine Disruptors and Male Fertility. Science. 308, 1466-1469;
- Ross Gillette, Isaac Miller-Crews, Michael K. Skinner, David Crews. (2015). Distinct actions of ancestral vinclozolin and juvenile stress on neural gene expression in the male rat. Front. Genet.. 6;
- T Colborn. (1995). Environmental estrogens: health implications for humans and wildlife.. Environmental Health Perspectives. 103, 135-136;
- Романцова Т.И. Эпидемия ожирения: очевидные и вероятные причины. (2011). «Ожирение и метаболизм». 1, 5-19;
- Antonia M. Calafat, Xiaoyun Ye, Lee-Yang Wong, John A. Reidy, Larry L. Needham. (2008). Exposure of the U.S. Population to Bisphenol A and 4- tertiary -Octylphenol: 2003–2004. Environmental Health Perspectives. 116, 39-44;
- Ronit Machtinger, Catherine M.H. Combelles, Stacey A. Missmer, Katharine F. Correia, Paige Williams, et. al.. (2013). Bisphenol-A and human oocyte maturation in vitro. Human Reproduction. 28, 2735-2745;
- Y. Ikezuki, O. Tsutsumi, Y. Takai, Y. Kamei, Y. Taketani. (2002). Determination of bisphenol A concentrations in human biological fluids reveals significant early prenatal exposure. Human Reproduction. 17, 2839-2841;
- M. Kundakovic, K. Gudsnuk, B. Franks, J. Madrid, R. L. Miller, et. al.. (2013). Sex-specific epigenetic disruption and behavioral changes following low-dose in utero bisphenol A exposure. Proceedings of the National Academy of Sciences. 110, 9956-9961;
- Jason G. Bromer, Yuping Zhou, Melissa B. Taylor, Leo Doherty, Hugh S. Taylor. (2010). Bisphenol-A exposure in utero leads to epigenetic alterations in the developmental programming of uterine estrogen response. The FASEB Journal. 24, 2273-2280;
- Ayami Matsushima. (2018). A Novel Action of Endocrine-Disrupting Chemicals on Wildlife; DDT and Its Derivatives Have Remained in the Environment. IJMS. 19, 1377;
- A H Wu, M C Yu, C-C Tseng, M C Pike. (2008). Epidemiology of soy exposures and breast cancer risk. Br J Cancer. 98, 9-14;
- K E Wynne-Edwards. (2001). Evolutionary biology of plant defenses against herbivory and their predictive implications for endocrine disruptor susceptibility in vertebrates.. Environmental Health Perspectives. 109, 443-448;
- National report on human exposure to environmental chemicals. (2018). CDC;
- А ты такой холодный, как… пластик в океане;
- I Lascombe, D Beffa, U Rüegg, J Tarradellas, W Wahli. (2000). Estrogenic activity assessment of environmental chemicals using in vitro assays: identification of two new estrogenic compounds.. Environmental Health Perspectives. 108, 621-629;
- T B Minh, M Watanabe, S Tanabe, T Yamada, J Hata, S Watanabe. (2001). Specific accumulation and elimination kinetics of tris(4-chlorophenyl)methane, tris(4-chlorophenyl)methanol, and other persistent organochlorines in humans from Japan.. Environmental Health Perspectives. 109, 927-935;
- Saba Rehman, Zeenat Usman, Sabeen Rehman, Moneera AlDraihem, Noor Rehman, et. al.. (2018). Endocrine disrupting chemicals and impact on male reproductive health. Transl. Androl. Urol.. 7, 490-503.
Источник Биомолекула.ру