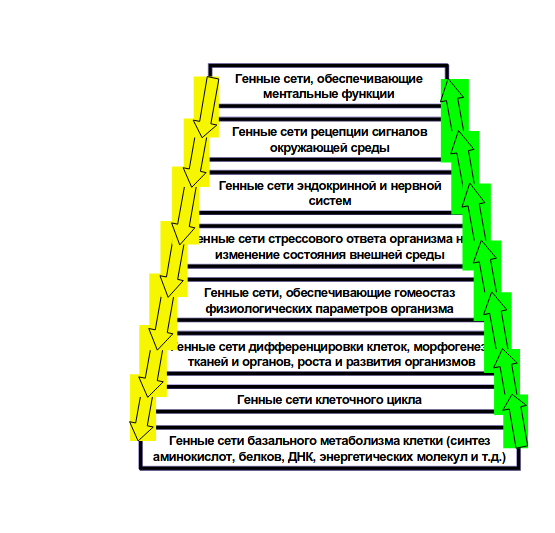
Иерархическая интеграция локальных генных сетей в общую генную сеть организма. Источник
Я люблю рассказывать, что социальное управляет биологическим как всадник лошадью: первое меняется по своим законам, открытым Бородачами и изученным разными иными исследователями, а второе «подстраивается» к его изменениям обычным путём, посредством отбора (всё время стабилизирующего). Таков «генетический след» арабской и европейской работорговли – повышенная частота замены Met на Thr в позиция 235 белка, кодируемого геном ангиотензиногена.
В приэкваториальных (не путать с тропическими) популяциях негров Африки, ведущих традиционно-первобытный образ жизни, это очень полезная адаптация. Они живут в условиях хронического дефицита микроэлементов: дожди, характерные для приэкваториальных экосистем, напрочь вымывают микроэлементы из почвы. Так единственным источником натрия оказываются сырые продукты охоты (для грудных детей – материнское молоко, поскольку животноводство невозможно, детей грудью кормят долго – до 5 лет, а потом еще какое-то время докармливают) или привозная – из Сахары — соль.
А вместе с нею приходила работорговля – обе профессии приватизировали арабы, уводившие рабов главным образом на север и восток. В итоге соленезависимые и “рабофобные” популяции накапливались на западе Африки — (Гвинейский залив и примыкающие к нему территории ~ соответствует красным территориям на карте). Но именно через Гвинейский залив в Африку проникли европейские работорговцы. Так сказать, с черного хода.
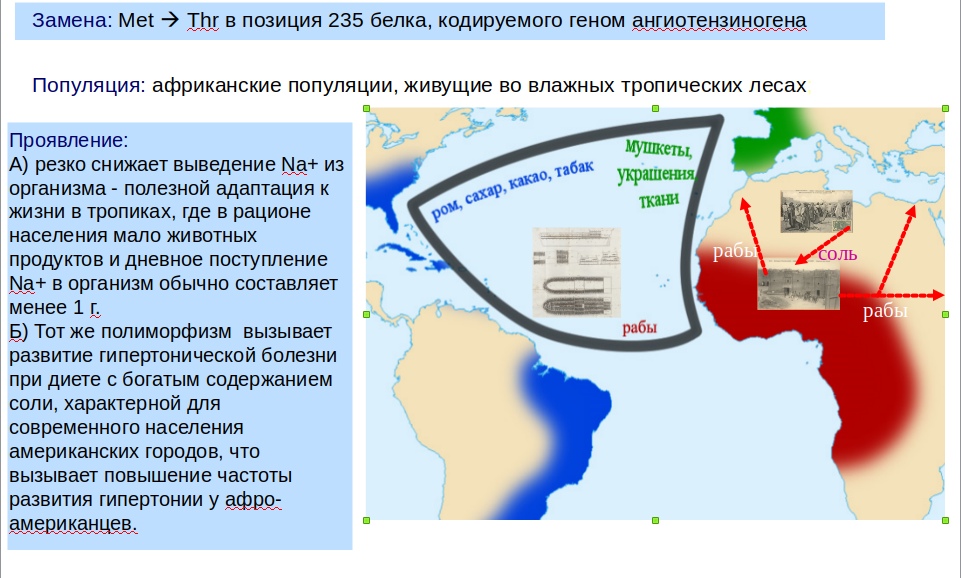 В итоге носителей указанного полиморфизма оказалось много среди американских негров, популяции которые уже давно не живут в приэкваториальных условиях и не добывают пропитание охотой и собирательством. Естественно, что у них полезный полиморфизм стал вредным, провоцирующим на фастфудной диете повышенный риск гипертонической болезни (опять относительность специфической адаптации, на сей раз при миграции – пусть вынужденной – в другую вмещающую экосистему). Отсюда видно, что адаптивная ценность мутации резко меняется при изменении природного ландшафта вокруг и режима питания. случавшихся всю человеческую историю» (Staessen J.A. et. аl., 1999).
В итоге носителей указанного полиморфизма оказалось много среди американских негров, популяции которые уже давно не живут в приэкваториальных условиях и не добывают пропитание охотой и собирательством. Естественно, что у них полезный полиморфизм стал вредным, провоцирующим на фастфудной диете повышенный риск гипертонической болезни (опять относительность специфической адаптации, на сей раз при миграции – пусть вынужденной – в другую вмещающую экосистему). Отсюда видно, что адаптивная ценность мутации резко меняется при изменении природного ландшафта вокруг и режима питания. случавшихся всю человеческую историю» (Staessen J.A. et. аl., 1999).
Замена Cys на Tyr в позиция 282 белка, кодируемого геном HFE, усиливающая эффективность абсорбции железа из пищи в кишечнике оказалась довольно частой среди западноевропейцев и восточных финноугорских народностей. В пожилом (пострепродуктивном) возрасте (50-70 лет) у носителей этой мутации наблюдается повышенный уровень железа в сердце, печени, поджелудочной железе, суставах, что ведет к дисфункции этих органов. Но в молодом (репродуктивном) возрасте повышенный уровень железа повышает иммунитет и выживаемость при сильной кровопотере (вместе дают устойчивость на рану). Естественно, что такой полиморфизм оказался полезным, а значит частым среди популяций, в комплекс традиционного поведения которых на определенном временном отрезке входили культы агрессии (скандинавы) или раны (традиционный менталитет кельтского воина предписывал презрение к защитному снаряжению).
Также считалось, что воин, не получивший раны в бою, сражался нечестно и презрение соотечественников обоего пола было ему обеспечено: масштаб раны должен был соответствовать масштабу победы (прямо по Симонову – “Да, враг был храбр. Тем больше наша слава” – отсюда летальное завершение истории Тристана и Изольды). По видимому, у этих популяций полиморфизм закрепился вследствие отбора среди мужчин.
 Ну а причем здесь неагрессивные финно-угры? Оказывается, у женщин-носительниц полиморфизма в репродуктивном возрасте повышенный уровень снижает риск железо-дефицитных состояний при беременности. Характерно, что замена оказалась распространенной не среди собственно финнов (они живут на Скандинавском докембрийском щите, где железа хоть отбавляй и где вместе с ними обитают потомки викингов), а среди угро-финских народностей, живущих гораздо восточнее (Thomas W. еt al., 1998).
Ну а причем здесь неагрессивные финно-угры? Оказывается, у женщин-носительниц полиморфизма в репродуктивном возрасте повышенный уровень снижает риск железо-дефицитных состояний при беременности. Характерно, что замена оказалась распространенной не среди собственно финнов (они живут на Скандинавском докембрийском щите, где железа хоть отбавляй и где вместе с ними обитают потомки викингов), а среди угро-финских народностей, живущих гораздо восточнее (Thomas W. еt al., 1998).
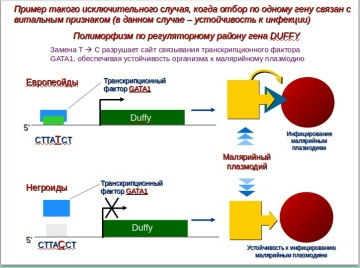
Случаи, когда фенотипический признак действительно в буквальном смысле определяется единственным геном и, больше того, даже единственным нуклеотидом в единственном сайте, большая редкость. Пример такого исключительного случая, когда отбор по одному гену связан с витальным признаком (устойчивости к инфекции) -полиморфизм по регуляторному району гена Duffy.
Замена T -> C разрушает сайт связывания транскрипционного фактора GATA1, обеспечивая устойчивость организма к малярийному плазмодию Plasmodium vivax, вызывающим трехдневную малярию. Частота такого полиморфизма оказалась высокой в популяциях негроидов, искони живших в очагах малярии, и пониженной в популяциях европейцев, впервые познакомившихся с малярией, вызываемыми P.vivax – трехдневной малярией — около начала нашей эры (Средиземноморье). Дальнейшее распространение различных малярий на север Европы было прервано малым ледниковым периодом Средневековья и лишь в XIX-XX в (появление центрального водяного отопления и теплых луж в зимних холодных подвалах, где размножаются комары), разные малярии начали осваивать европейский континент.
В гетерозиготе указанный полиморфизм дает преимущество – устойчивость к P.vivax, однако в гомозиготе смертелен (болезнь серповидноклеточная анемия), поэтому отбор здесь в пользу гетерозигот. Открытие этого факта стало одним из доводов в пользу синтетической теории эволюции (СТЭ), занимающей ныне доминирующую позицию.
А дальше неожиданно выяснилось, что ген Duffy абсолютно необходим для защиты от Plasmodium falciparum – возбудителя тропической малярии, известной также как малярия вообще. Получается, защищаясь от Plasmodium vivax, человеческие популяции “подставляются” Plasmodium falciparum; поэтому обычная малярия у негроидов протекает тяжелее, чем у европеоидов, а трехдневная – наоборот. Кроме мутации в сайте связывания GATA1 в промоторе гена Duffy, различные популяции негроидов несут множество полиморфизмов так или иначе снижающих экспрессию данного гена – вплоть до полного его выключения. Однако изменение эпидемиологической обстановки с легко лишит адаптивной ценности такие мутации.
Другой похожий пример — мононуклеотидная делеция остатка фенилаланина ΔF508, но только не в регуляторной некодирующей части, а в белоккодирующем регионе гена СF. Его белок CFTR – один из транспортеров ионов хлора через клеточную (внешнюю или внутреннюю, например, эндоплазматический ретикулум) мембрану. Делеция фенилаланина ведет к дефектам встраивания белка в мембрану и к нестабильности нативной 3D –cтруктуры встроившегося белка. Повышенное содержание хлора в жидкостях тела, равно как и повышенное содержание самих жидкостей в полостях тела у гетерозигот способствует выживанию при таких инфекционных болезнях, как холера и чума. Но у гомозигот развивается муковисцидоз – неинфекционное заболевание. Связанное с отеками множества органов, что ведет к их дисфункции и к быстрой гибели без поддерживающей терапии.
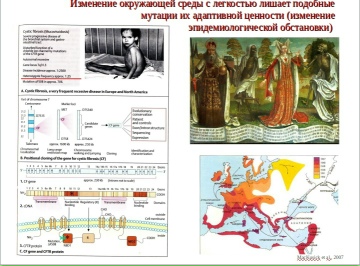
Важно отметить, что в популяциях европейцев, происходящих с территорий Западной Европы, подвергшихся опустошительным эпидемиям чумы («Черная Смерть») в Средние века частота полиморфизма ΔF508 до сих пор очень высока. В популяциях евреев-ашкеназим, живших с ними одновременно на тех же территориях, с высокой частотой присутствуют другие полиморфизмы, также ведущие к муковисцидозу в гомозиготе, что отражает репродуктивный барьер между еврейским и христианским населением, так что общий фактор отбора затрагивает разный генный субстрат.
Для дальнейшего также важно отметить, что на этом примере как на предыдущем хорошо видна относительность любой специфической (то есть направленной на адаптацию к конкретному фактору внешней среды) адаптации. Конкретный фактор – опустошительные эпидемии — в Западной Европе не действует минимум 200 лет, а популяция до сих пор платит кровавую цену адаптации. Так последняя пандемия холеры была остановлена на Волге в 1980 гг. ХХ в., а зародилась за 30 лет до этого в Ю.-В. Азии (где и нанесла большой ущерб, переболел каждый третий) после обвала санитарной службы вместе с породившей ее колониальной системой. Источник — (McKusick et al., 2007).
Однако случай “одна мутация — одна уязвимость или напротив, устойчивость к болезни) – редкость. В определении того, что будет на выходе, уязвимость или устойчивость к болезням и иным факторам не благоприятности, контекст много важней собственно изменений в геноме. Популярно об этом же см. Моалем Шарон «А если они нам не враги?» про эволюционный взгляд на болезни как неизбежное следствие относительности адаптации, особенно в условиях быстрых изменений образа жизни людей.
Что отсюда следует для теории эволюции?
Гены в организме не изолированы, как верят читатели «Эгоистичного гена» Р.Докинза, а связаны регуляторными взаимодействиями в батареи, так называемые генные сети. В рамках сетей они работают — а также эволюционируют - вместе, управляемые организмом как целым.
Генная сеть — группа координированно функционирующих генов, обеспечивающих формирование определенного фенотипического признака организма (молекулярного, биохимического, физиологического, морфологического, поведенческого и т.д.). Иными словами, чем сложнее организм, тем чаще эволюционирует не ген, а полигенный фенотипический признак. Добраться до отдельных генов отбору удается лишь в исключительных случаях [и именно в них, как дальше увидим, полигенность видна особенно хорошо]. Т.е. на эволюцию генных сетей распространяется парадокс результата (У.Найсер, 1981) – верный (=адаптивный) результат редко несет информацию о пути к своему достижению.
Даже в самых, казалось бы, простых случаях (отбор по одному гену), на самом деле отбирается некая генная сеть. Один и тот же ген (по крайней мере у эукариот) может эволюционировать в составе разных генных сетей. Отбор по одному гену или даже по нескольким генам в СТЭ – удобное упрощение (типа идеального газа), облегчающее расчеты в популяционной генетике. Часто такое упрощение оправдывается практикой или позволяет теоретически исследовать различные варианты эволюции в предельно ”чистом виде”. Но не всегда…
Хотя один и тот же полиморфизм (генный вариант) в примерах выше оказывается адаптивен в двух разных популяциях, однако фактически отбор шёл по совершенно различным признакам фенотипа и – соответственно — по разным генным сетям (парадокс результата!);
Один и тот тот же полиморфизм в наших примерах был адаптивен на одном временном отрезке онтогенеза и дезадаптивен – на другом (антагонизм, сбалансированный по времени онтогенеза). И в этом случае в разные периоды онтогенеза отбор был фактически связан с разными генными сетями, каждая из которых включала ген HFE;
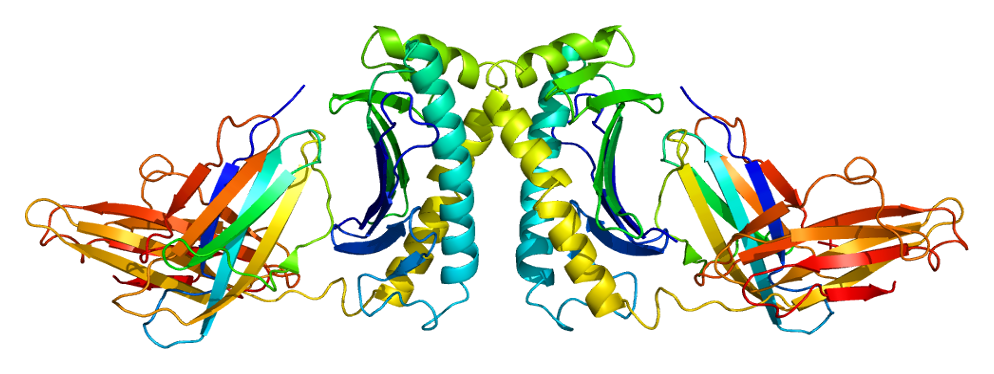
HFE — трансмембранный белок, регулирующий метаболизм железа. Связывается с рецептором трансферрина 1 (TFR1), блокируя избыточное поступление железа в клетки
Резюмируя: хотя отбор может оценивать один и тот же ген, результат оценки может очень сильно зависеть от того в составе какой генной сети этот ген работает. И когда один ген эволюционирует в составе разных регуляторных контуров (т.е. генных сетей) результат оказывается очень различным. Впервые экспериментально это показал Камшилов в опытах с мутацией eyeless в 1939-1941 гг.
Источник: лекции нс ИЦиГ В.В.Суслова, прочитанные в 2020 г на кафедре информационной биологии НГУ в рамках магистерского спецкурса Ю.Г.Матюшкина “Эволюционная биология. I. Теория молекулярной эволюции». Пересказ публикуется с любезного разрешения автора.